题目内容
关于乙醇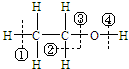 在化学反应中断键位置说法错误的是( )
在化学反应中断键位置说法错误的是( )
 在化学反应中断键位置说法错误的是( )
在化学反应中断键位置说法错误的是( )| A、乙醇在铜催化下与氧气反应,在②④位置断裂,所以只有与羟基直接相连的碳原子上有氢原子才能发生催化氧化 |
| B、乙醇与钠反应,在④位置断裂 |
| C、乙醇与浓硫酸在140℃时,在③或④位置断裂,该反应属于取代反应 |
| D、乙醇与浓硫酸在170℃时,在②③位置断裂,以水分子的形式消去,属于消去反应 |
考点:乙醇的化学性质
专题:有机反应
分析:A.乙醇在铜催化下与氧气反应生成乙醛,断裂的是羟基上的氢氧键、与羟基所连的碳上的碳氢键;
B.乙醇与金属钠反应生成乙醇钠和氢气,断开的是羟基上的氢氧键;
C.乙醇和浓H2SO4共热至140℃时,发生分子间脱水,断开的是羟基上的氢氧键、碳氧键;
D.乙醇和浓H2SO4共热至170℃时发生消去反应,断裂碳氧键、与羟基所连的碳的相邻的碳上的碳氢键.
B.乙醇与金属钠反应生成乙醇钠和氢气,断开的是羟基上的氢氧键;
C.乙醇和浓H2SO4共热至140℃时,发生分子间脱水,断开的是羟基上的氢氧键、碳氧键;
D.乙醇和浓H2SO4共热至170℃时发生消去反应,断裂碳氧键、与羟基所连的碳的相邻的碳上的碳氢键.
解答:
解:A.乙醇在铜催化下与氧气反应生成乙醛,断裂的是羟基上的氢氧键、与羟基所连的碳上的碳氢键,断键的位置为②④,故A正确;
B.乙醇与与金属钠反应生成乙醇钠和氢气:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,故乙醇断键的位置为④,故B正确;
C.乙醇和浓H2SO4共热至140℃时,发生分子间脱水2CH3CH2OH
CH3CH2OCH2CH3+H2O,故乙醇断键的位置为③和④,故C正确;
D.乙醇和浓H2SO4共热至170℃时,发生消去反应,生成乙烯,反应方程式为CH3CH2OH
CH2═CH2↑+H2O,故乙醇断键的位置为①和③,故D错误,
故选D.
B.乙醇与与金属钠反应生成乙醇钠和氢气:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,故乙醇断键的位置为④,故B正确;
C.乙醇和浓H2SO4共热至140℃时,发生分子间脱水2CH3CH2OH
| 浓硫酸 |
| 140℃ |
D.乙醇和浓H2SO4共热至170℃时,发生消去反应,生成乙烯,反应方程式为CH3CH2OH
| 浓硫酸 |
| 170℃ |
故选D.
点评:本题主要考查了乙醇的化学性质,掌握有机化学反应中断键的位置是解答的关键,难度不大.

练习册系列答案
 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
下列说法不正确的是( )
| A、霾的形成与PM2.5有直接关系 |
| B、自行车钢架生锈主要是电化学腐蚀所致 |
| C、用加热的方法杀死H7N9禽流感病毒是采用了蛋白质变性原理 |
| D、人类在研究物质微观结构的过程中,扫描隧道显微镜、光学显微镜、电子显微镜先后得到了使用 |
部分弱酸的电离平衡常数如表,表述肯定正确的是( )
| 弱酸 | H2CO3 | H2SO3 | HClO |
| 电离平衡常数 (25℃) |
K1=4.30×10-7 | K1=1.54×10-2 | K=2.95×10-8 |
| K2=5.61×10-11 | K2=1.02×10-7 |
| A、相同温度时三种溶液的pH关系:Na2CO3>NaClO>Na2SO3 |
| B、ClO-+H2O+CO2→HClO+HCO3- |
| C、2ClO-+SO2+H2O→2HClO+SO32- |
| D、等体积、等物质的量浓度的HClO 和Na2CO3混合后溶液呈碱性 |
常温下,下列各组离子在溶液中一定能大量共存的是( )
| A、Ca2+、K+、CO32-、Cl- |
| B、K+、NH4+、HCO3-、OH- |
| C、H+、Fe2+、ClO-、SO42- |
| D、Na+、Ba2+、OH-、NO3- |
下列物质的水溶液因发生水解而显酸性的是( )
| A、NH4Cl |
| B、KHSO4 |
| C、NaHCO3 |
| D、H2SO4 |
化学与社会、生产、生活紧切相关.下列说法正确的是( )
| A、PM2.5颗粒直径约是原子直径的2.5倍 |
| B、淀粉、蔗糖、氨基酸在一定条件都能发生水解反应 |
| C、植物油通常能和氢氧化钠溶液发生反应 |
| D、应该倡议禁止向绿色食品中添加任何化学物质 |
