题目内容
2.分类是化学研究的重要方法之一,下列有关说法中,正确的是( )| A. | SO2、NO2和CO2都属于酸性氧化物 | |
| B. | 甲烷和和一氯甲烷都属于烷烃 | |
| C. | 碱性氧化物都是金属氧化物 | |
| D. | 在水溶液中能电离出H+的化合物都属于酸 |
分析 A.酸性氧化物是指能与碱反应生成盐和水的氧化物;
B.烷烃属于烃类,组成元素只有碳元素和氢元素;
C.碱性氧化物是和酸反应生成盐和水的氧化物,发生的是复分解反应;
D.在水溶液中能电离出的阳离子全部是H+的化合物属于酸.
解答 解:A、二氧化氮不属于酸性氧化物,SO2和CO2都属于酸性氧化物,故A错误;
B、甲烷和属于烷烃,但是一氯甲烷中含有氯元素,不属于烷烃,属于卤代烃,故B错误;
C.碱性氧化物是和酸反应生成盐和水的氧化物,碱性氧化物都是金属氧化物,故C正确;
D、只有在水溶液中能电离出的阳离子全部是H+的化合物才属于酸,如硫酸氢钠在水溶液中能电离出氢离子,但是属于盐,故D错误.
故选C.
点评 本题考查学生物质分类的有关知识,注意知识的归纳和整理是关键,概念的掌握要灵活,难度中等.

练习册系列答案
相关题目
4.某老师批阅学生实验报告,下列哪些学生是以科学的态度记录实验数据的( )
| A. | 甲学生用50mL量筒量取46.70mL浓盐酸 | |
| B. | 乙学生用广泛pH试纸测定溶液的酸碱性:pH=14.5 | |
| C. | 丙学生配NaOH溶液,用电子天平称取固体1.220g | |
| D. | 丁学生用红柄滴定管量取25.00mL0.1mol/L的盐酸 |
13.化学理论在元素单质及其化合物反应中应用广泛.
(1)在一定条件下,可逆反应mA?nB+pC△H,达到平衡状态.
①若A、B、C都是气体,增大压强,平衡向正反应方向移动,则m大于n+p(填“大于”、“小于”或“等于”).
②其他条件不变,加热后A的质量减小,则反应△H大于0(填“大于”、“小于”或“等于”).
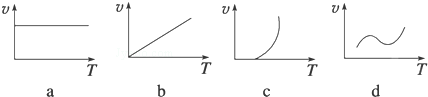
(2)某些金属氧化物(如FeXOY)粉末和Al粉在镁条的引燃下可以发生铝热反应,下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是c
(3)一定温度下,发生反应:FeO(s)+CO(g)?Fe(s)+CO2(g)△H.已知该反应在不同温度下的平衡常数如下表:
请回答下列问题:
①该反应的△H<0(填“>”、“<”或“=”).
②T℃时,将FeO(s)和CO(g)各3.0mol加入10L的密闭容器中,反应达到平衡后,测得CO转化率为W1,c(CO2)=0.15mol•L-1,则温度T低于(填“高于”、“低于”、“等于”)1000,若此时保持其它条件不变再充入2.0mol CO(g),再达平衡时测得CO转化率为W2,则W1=W2(填“>”、“<”或“=”).
(1)在一定条件下,可逆反应mA?nB+pC△H,达到平衡状态.
①若A、B、C都是气体,增大压强,平衡向正反应方向移动,则m大于n+p(填“大于”、“小于”或“等于”).
②其他条件不变,加热后A的质量减小,则反应△H大于0(填“大于”、“小于”或“等于”).
(2)某些金属氧化物(如FeXOY)粉末和Al粉在镁条的引燃下可以发生铝热反应,下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是c

(3)一定温度下,发生反应:FeO(s)+CO(g)?Fe(s)+CO2(g)△H.已知该反应在不同温度下的平衡常数如下表:
| 温度/℃ | 1000 | 1100 |
| 平衡常数 | 0.68 | 0.50 |
①该反应的△H<0(填“>”、“<”或“=”).
②T℃时,将FeO(s)和CO(g)各3.0mol加入10L的密闭容器中,反应达到平衡后,测得CO转化率为W1,c(CO2)=0.15mol•L-1,则温度T低于(填“高于”、“低于”、“等于”)1000,若此时保持其它条件不变再充入2.0mol CO(g),再达平衡时测得CO转化率为W2,则W1=W2(填“>”、“<”或“=”).
17.维生素C的结构简式为: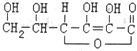 ,有关它的叙述不正确的是( )
,有关它的叙述不正确的是( )
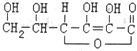 ,有关它的叙述不正确的是( )
,有关它的叙述不正确的是( )| A. | 在碱性溶液中能稳定存在 | |
| B. | 容易发生氧化反应和加成反应 | |
| C. | 可以溶解于水,溶液显酸性 | |
| D. | 可以看作环状酯类化合物,分子式为C6H8O6 |
11.下列对溶液叙述正确的是( )
| A. | 在中和滴定实验中,容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管用蒸馏水洗净后,须经干燥或润洗后方可使用 | |
| B. | 对于pH相同的氢氧化钠和氨水,加水稀释至m倍和n倍后,若稀释后溶液的pH相等,则m>n | |
| C. | 向冰醋酸中加水至配成醋酸稀溶液的过程中H+的浓度逐渐减小 | |
| D. | 25℃时NH4Cl溶液的KW大于100℃时NaCl溶液的KW |




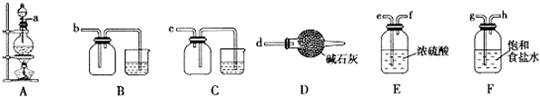
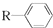 $→_{一定条件}^{CO、HCl}$
$→_{一定条件}^{CO、HCl}$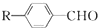 ,为合成某种液晶材料的中间体M,有人提出如下不同的合成途径:
,为合成某种液晶材料的中间体M,有人提出如下不同的合成途径: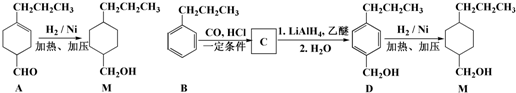
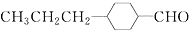 和
和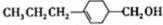 (写结构简式)生成.
(写结构简式)生成.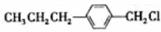 .
.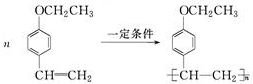 .
.