题目内容
设NA表示阿伏加德罗常数的值。下列说法正确的是
| A.45gHCHO与CH3COOH混合物含氢原子数为3NA |
| B.常温常压下,54g重水(D2O)含水分子数为3NA |
| C.标准状况下,11.2L苯含有C-H键数目为3NA |
| D.反应KIO3+6HI=3I2+KI+3H2O,每生成1.5mol I2转移电子数为3NA |
A
解析试题分析:A、HCHO与CH3COOH的可以写成通式(CH2O)n,相对分子质量为30n,混合物中含有H原子: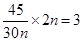 ,正确;B、D2O的相对分子质量为20,54g D2O的物质的量为2.7mol,错误;C、苯为液体,不适用于标准状况的气体摩尔体积,错误;D、生成3mol I2时,转移5 mol 电子,错误。
,正确;B、D2O的相对分子质量为20,54g D2O的物质的量为2.7mol,错误;C、苯为液体,不适用于标准状况的气体摩尔体积,错误;D、生成3mol I2时,转移5 mol 电子,错误。
考点:阿伏伽德罗常数

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
下列说法正确的是
| A.2 mol/L KCl溶液与1 mol/L K2SO4溶液混合后,c(K+)为2 mol/L |
| B.120 g NaCl溶液中溶有20 g NaCl,该温度下NaCl的溶解度为20g |
| C.22.4 L HCl气体溶于水制成1 L溶液,该溶液的物质的量浓度为1 mo1/L |
| D.把5 g胆矾(CuSO4?5H2O)溶于45 g水中,所得溶液溶质的质量分数为10% |
设NA是阿伏伽德罗常数的数值,下列说法正确的是
| A.0.1mo1·L-1MgCl2溶液中含C1一数为0.2 NA |
| B.1 L 0.1m01.L-1Al C13溶液中,Al3+数为0.1NA |
| C.标准状况下,22.4L的CCl4中含CCl4分子数为NA |
| D.1mol铁与足量的C12反应,转移的电子数为3NA |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.1mol 1-丁炔中,含2NA个π键,9NA个σ键 |
| B.在O2参与的反应中,1mol O2作氧化剂时得到的电子数一定是4NA |
| C.22.4LHC1溶于水时,有NA个共价键发生断裂 |
| D.17 g甲基(-14CH3)所含电子数为10NA |
下列有关化学用语表示正确的是
A.氢氧化钠的电子式: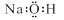 |
B.Cl-的结构示意图: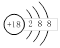 |
C.2-丁醇的结构简式: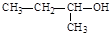 |
| D.碳酸的电离方程式:H2CO3=2H++CO32- |
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.常温下,40gSO3含有1.5NA个氧原子 |
| B.1L 0.1mol/L的醋酸溶液中含有0.1NA个H+ |
| C.标准状况下,22.4L CCl4含有4NA个C—C1键 |
| D.lmolNa与足量的H2O反应,转移2NA个电子 |
已知:2Fe+3Cl2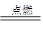 2FeCl3,下列说法正确的是(设nA为阿伏加德罗常数的数值)
2FeCl3,下列说法正确的是(设nA为阿伏加德罗常数的数值)
| A.氯气是氧化剂,FeCl3是还原剂 |
| B.常温下,与56g Fe反应断裂1.5 nA个Cl—Cl键 (相对原子质量:Fe-56) |
| C.1 L 0.1 mol?L-1 FeCl3溶液中含有0.1 nA个Fe3+ |
| D.常温常压下,22.4 L的Cl2和足量Fe反应转移3 nA个电子 |
设nA为阿伏加德罗常数的数值,下列说法正确的是
| A.常温下,14gC2H4含有nA个氢原子 |
| B.1mol C和足量浓硫酸完全反应转移4nA个电子 |
| C.1L 0.1mol·L-1的Na2CO3溶液含有0.1nA个CO32- |
| D.标准状况下,22.4L CH3CH2OH含有个nA个CH3CH2OH分子 |