题目内容
设nA为阿伏加德罗常数的数值,下列说法正确的是
| A.常温下,14gC2H4含有nA个氢原子 |
| B.1mol C和足量浓硫酸完全反应转移4nA个电子 |
| C.1L 0.1mol·L-1的Na2CO3溶液含有0.1nA个CO32- |
| D.标准状况下,22.4L CH3CH2OH含有个nA个CH3CH2OH分子 |
B
解析试题分析:乙烯的相对分子质量为28,由于n=m/M,则乙烯的物质的量为0.5mol,由于关系式:C2H4~4H中两物质的系数之比等于物质的量之比,则氢原子的物质的量为2mol,氢原子为2nA,故A错误;碳和浓硫酸发生氧化还原反应,由于C+2H2SO4(浓)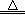 CO2↑+2SO2↑+2H2O~4e-中各物质的系数之比等于物质的量之比,则1molC和足量浓硫酸完全反应转移4mol电子,故B正确;由于n=c?V,则碳酸钠的物质的量为0.1mol,由于碳酸钠是强碱弱酸盐,虽然0.1mol碳酸钠完全电离出0.1mol碳酸根离子,但是碳酸根离子能部分水解,则溶液中剩余的碳酸根离子小于0.1mol,故C错误;虽然 n=V/Vm,标准状况下气体摩尔体积为22.4L/mol,但是乙醇是液体,不能该公式求其物质的量,其物质的量不是1mol,故D错误。
CO2↑+2SO2↑+2H2O~4e-中各物质的系数之比等于物质的量之比,则1molC和足量浓硫酸完全反应转移4mol电子,故B正确;由于n=c?V,则碳酸钠的物质的量为0.1mol,由于碳酸钠是强碱弱酸盐,虽然0.1mol碳酸钠完全电离出0.1mol碳酸根离子,但是碳酸根离子能部分水解,则溶液中剩余的碳酸根离子小于0.1mol,故C错误;虽然 n=V/Vm,标准状况下气体摩尔体积为22.4L/mol,但是乙醇是液体,不能该公式求其物质的量,其物质的量不是1mol,故D错误。
考点:考查阿伏加德罗常数,涉及质量、摩尔质量、物质的量、物质的组成、氧化还原反应中转移电子数、物质的量浓度、溶液体积、盐类水解、气体摩尔体积、非气态物质等。

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
化学用语是学习化学的重要工具,下列表示物质变化的化学用语中,正确的是
A.BaSO4悬浊液中存在平衡:BaSO4(aq)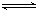 Ba2+(aq)+SO42-(aq) Ba2+(aq)+SO42-(aq) |
B.向K2Cr2O7溶液中加入少量NaOH浓溶液,溶液由橙色变为黄色:Cr2O72-+H2O 2CrO42-+2H+ 2CrO42-+2H+ |
| C.等浓度的NH4Al(SO4)2溶液与Ba(OH)2溶液以1:2体积比混合出现白色沉淀:Al3++2SO42-+2Ba2++3OH-=2BaSO4↓+Al(OH)3↓ |
D.铝热反应的原理为:Al2O3+2Fe 2Al+Fe2O3 2Al+Fe2O3 |
设NA表示阿伏加德罗常数的值。下列说法正确的是
| A.45gHCHO与CH3COOH混合物含氢原子数为3NA |
| B.常温常压下,54g重水(D2O)含水分子数为3NA |
| C.标准状况下,11.2L苯含有C-H键数目为3NA |
| D.反应KIO3+6HI=3I2+KI+3H2O,每生成1.5mol I2转移电子数为3NA |
下列化学用语书写正确的是
A.NaHS水解反应:HS-+ H2O H3O++ S2- H3O++ S2- |
B.用两个铜片作电极电解盐酸的初始阶段:Cu+2H+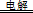 H2↑+Cu2+ H2↑+Cu2+ |
| C.Fe3O4与稀硝酸反应:Fe3O4+8H+ = Fe2++2Fe3++4H2O |
| D.碳酸氢钠溶液中加入过量Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+CO32-+2H2O |
设nA是阿伏加德罗常数的数值。下列说法正确的是
| A.1L 0.1mol·L-1的FeCl3溶液中,Fe3+的数目为0.1nA |
| B.1molNH3中含有N-H键的数目为3nA |
| C.7.8g Na2O2中含有的阳离子数目为0.1nA |
| D.标准状况下,22.4L水中分子个数为nA |
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.1L0.1mol·L-1NaHSO3溶液中含有H+的数目为NA个 |
| B.常温常压下,等质量的CO2和N2O的气体体积相等 |
| C.60g组成为C2H4O2的有机物含C-H键数目为3NA个 |
| D.向稀HNO3溶液中加入过量的铁粉经充分反应后,转移的电子数目为3NA个 |
下列有关化学用语表示正确的是
| A.Mg2+的电子排布式:1s22s22p63s2 |
B.铁的原子结构示意图: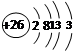 |
C.Na2S的电子式: 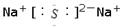 |
| D.次氯酸的结构式:H-Cl-O |
下列说法不正确的是(设NA为阿伏加德罗常数的数值)( )
| A.20g重水含有10NA个电子 |
| B.1L 0.1 mol·L-1 Na2SO3溶液中含有的SO32-数目少于0.1NA个 |
| C.使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏高 |
| D.用足量铜粉除去FeCl2溶液中的FeCl3杂质 |
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.46 g乙醇中含有的化学键数为7 NA |
| B.1 mol氯气和足量NaOH溶液反应转移电子数为2 NA |
| C.1 mol OH-和1 mol -OH(羟基)中含有的质子数均为 9 NA |
| D.10 L 0.1 mol·L-1的Na2CO3溶液中,Na+、CO32-总数为3 NA |