题目内容
已知Q与R的摩尔质量之比为9:22。在反应X+2Y
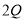 +R中,当1.6g X与Y完全反应后,生成4.4g R,则参与反应的Y和生成物
+R中,当1.6g X与Y完全反应后,生成4.4g R,则参与反应的Y和生成物 的质量比为
的质量比为
A.46:9 B.32:9 C.23:9 D.16:9
练习册系列答案
相关题目
18.X、Y、Z、W四种常见元素,其中X、Y、Z为短周期元素.有关信息如表:
(1)W在周期表的位置为第四周期第Ⅷ族,W(OH)2在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3.
(2)X的简单阴离子的结构示意图为 ,X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为6H++Al2O3=2Al3++3H2O.
,X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为6H++Al2O3=2Al3++3H2O.
(3)Z的氧化物在通讯领域用来作光导纤维,工业上制备Z的单质的化学反应方程式为SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
锗与Z是同一主族元素,门捷列夫曾预言了这一元素的存在,它用来制造半导体晶体管,最新研究表明:有机锗具有明显的抗肿瘤活性,锗不与NaOH 溶液反应但在有H2O2 存在时可与NaOH 溶液反应生成锗酸盐,其方程式为Ge+2 H2O2+2NaOH=Na2GeO3+3H2O.
(4)在50mL l mol•L-1的YX3溶液中逐滴加入0.5mol•L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积可能二种情况(填一或二).
| 原子或分子相关信息 | 单质及其化合物相关信息 | |
| X | ZX4分子是由粗Z提纯Z的中间产物 | X的最高价氧化物对应的水化物为无机酸中最强酸 |
| Y | Y原子的最外层电子数等于电子层数 | Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料 |
| Z | Z原子的最外层电子数是次外层电子数的$\frac{1}{2}$ | Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料 |
| W | W原子的最外层电子数小于4 | W的常见化合价有+3、+2,WX3稀溶液呈黄色 |
(2)X的简单阴离子的结构示意图为
 ,X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为6H++Al2O3=2Al3++3H2O.
,X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为6H++Al2O3=2Al3++3H2O.(3)Z的氧化物在通讯领域用来作光导纤维,工业上制备Z的单质的化学反应方程式为SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
锗与Z是同一主族元素,门捷列夫曾预言了这一元素的存在,它用来制造半导体晶体管,最新研究表明:有机锗具有明显的抗肿瘤活性,锗不与NaOH 溶液反应但在有H2O2 存在时可与NaOH 溶液反应生成锗酸盐,其方程式为Ge+2 H2O2+2NaOH=Na2GeO3+3H2O.
(4)在50mL l mol•L-1的YX3溶液中逐滴加入0.5mol•L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积可能二种情况(填一或二).
19.下列离子方程式正确的是( )
| A. | 石灰石溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | CuCl2溶液中投入单质Na:2Na+Cu2+═2Na++Cu | |
| C. | FeCl3溶液中投入单质Cu:Fe3++Cu═Fe2++Cu2+ | |
| D. | 碳酸氢钠溶液与少量澄清石灰水反应:HCO3-+Ca2++2OH-═CaCO3↓+H2O+CO32- |


 =____________________________.
=____________________________. 、
、 、
、 、
、 、
、 、
、 六种微粒。其中
六种微粒。其中
 还原剂,转移
还原剂,转移 电子
电子 D.1mol CH3COOK约含有3×6.02×1023个H
D.1mol CH3COOK约含有3×6.02×1023个H