题目内容
下列离子方程式中,正确的是( )
| A、稀硫酸与NaOH溶液反应2H++OH-=H2O |
| B、AgNO3溶液与NaCl溶液反应 Ag++Cl-=AgCl↓ |
| C、CaCO3与稀盐酸反应 CO32-+2H+=CO2↑+H2O |
| D、Fe片插入FeCl3溶液中 Fe+Fe3+=2Fe2+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.电荷不守恒,氢原子个数不守恒;
B.AgNO3和与NaCl都可溶,AgCl是难溶物;
C.碳酸钙是难溶物;
D.电荷不守恒.
B.AgNO3和与NaCl都可溶,AgCl是难溶物;
C.碳酸钙是难溶物;
D.电荷不守恒.
解答:
解:A、电荷不守恒,氢原子个数不守恒,应为:H++OH-=H2O,故A错误;
B、AgNO3和与NaCl都可溶,AgCl是难溶物,符合离子方程式的书写要求,故B正确;
C、碳酸钙是难溶物,不可拆分,应为:CaCO3+-+2H+=Ca2++CO2↑+H2O,故C错误;
D、电荷不守恒,应为:Fe+2Fe3+=3Fe2+,故D错误;
故选:B.
B、AgNO3和与NaCl都可溶,AgCl是难溶物,符合离子方程式的书写要求,故B正确;
C、碳酸钙是难溶物,不可拆分,应为:CaCO3+-+2H+=Ca2++CO2↑+H2O,故C错误;
D、电荷不守恒,应为:Fe+2Fe3+=3Fe2+,故D错误;
故选:B.
点评:离子方程式的书写是高考不变的一个题型,每年高考必考,是热点题型,题目难度不大.本题重点是电荷是否守恒.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
关于3mol CO2的说法正确的是( )
| A、质量为44g |
| B、有6mol O |
| C、分子数为6.02×1023 |
| D、相对分子质量为44g/mol |
下列物质属于钠盐的是( )
| A、Na2O |
| B、Na2O2 |
| C、NaOH |
| D、CH3COONa |
下列物质类别、名称(或俗名)、化学式相符的是( )
| A、碱性氧化物,氧化亚铁,Fe2O3 |
| B、酸,硫酸,H2SO3 |
| C、碱,熟石灰,CaO |
| D、酸性氧化物,干冰,CO2 |
下列说法不正确的是( )
| A、等质量的乙烷、乙烯、乙炔完全燃烧耗氧量依次减小 |
| B、CnH2n+1-Br的沸点随分子中碳原子数增多而升高,相对密度则减小 |
| C、苯分子中所有化学键键长、键能、键角都相同 |
| D、等物质的量的甲烷、醋酸完全燃烧耗氧量相等 |
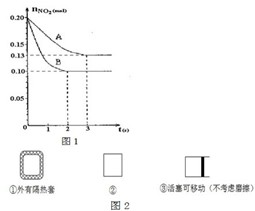 在容积为VL的密闭容器中发生2NO2?2NO+O2反应.反应过程中NO2的物质的量随时间变化的状况如图1所示.
在容积为VL的密闭容器中发生2NO2?2NO+O2反应.反应过程中NO2的物质的量随时间变化的状况如图1所示.