题目内容
16.每组中都有一种物质与其他物质在分类上或性质上不同,试分析每组中物质的组成规律或性质特点,将这种物质找出来,并说明理由.①O2CO H2 MgCO,CO由不同元素组成,其余物质只有一种元素组成;
②CO2SO3 CO CaOCaO,CaO是金属元素和氧元素组成的,其余的是非金属元素和氧元素组成的.
分析 ①O2、H2、Mg只有一种元素组成,CO由不同元素组成;
②CO2、SO3、CO 是非金属元素和氧元素组成的,CaO是金属元素和氧元素组成的.
解答 解:①O2、H2、Mg只有一种元素组成,CO由不同元素组成,CO与其他物质在分类上或性质上不同,
故答案为:CO;CO由不同元素组成,其余物质只有一种元素组成;
②CO2、SO3、CO 是非金属元素和氧元素组成的,CaO是金属元素和氧元素组成的,
故答案为:CaO;CaO是金属元素和氧元素组成的,其余的是非金属元素和氧元素组成的.
点评 本题考查了物质的分类问题,掌握物质的分类标准是解题关键,题目难度不大.

练习册系列答案
相关题目
7.在标准状况下,VL氯化氢气体溶于1L水中,所得溶液的密度为ρ g•cm-3,溶质的质量分数为ω.则此溶液的物质的量浓度为( )
| A. | $\frac{1000ωνρ}{36.5}$mol/L | B. | $\frac{1000νρ}{36.5+22400}$mol/L | ||
| C. | $\frac{ων}{22.4(V+1)}$mol/L | D. | $\frac{1000νρ}{36.5V+22400}$mol/L |
8.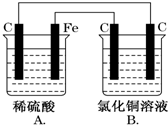 烧杯A中盛放0.1mol•L-1的H2SO4溶液,烧杯B中盛放0.1mol•L-1的CuCl2溶液(两种溶液均足量),装置如图所示,下列说法不正确的是( )
烧杯A中盛放0.1mol•L-1的H2SO4溶液,烧杯B中盛放0.1mol•L-1的CuCl2溶液(两种溶液均足量),装置如图所示,下列说法不正确的是( )
 烧杯A中盛放0.1mol•L-1的H2SO4溶液,烧杯B中盛放0.1mol•L-1的CuCl2溶液(两种溶液均足量),装置如图所示,下列说法不正确的是( )
烧杯A中盛放0.1mol•L-1的H2SO4溶液,烧杯B中盛放0.1mol•L-1的CuCl2溶液(两种溶液均足量),装置如图所示,下列说法不正确的是( )| A. | A为原电池,B为电解池 | |
| B. | A中阳离子向碳极移动,阴离子向铁极移动 | |
| C. | 当A烧杯中产生0.1 mol气体时,B烧杯中产生气体的物质的量也为0.1 mol | |
| D. | 一段时间后,B烧杯中溶液的浓度增大 |
6.在CO(g)+H2O(g)?CO2(g)+H2(g)(正反应为放热反应)反应中,改变下列条件,不能使v正增大的是( )
| A. | 升高温度 | B. | 使用催化剂 | C. | 降低温度 | D. | 缩小容器体积 |
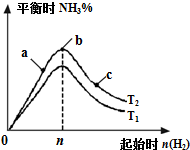 某科研小组研究在其他条件不变的情况下,改变起始氢气物质的量[用n(H2)表示]对N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol 反应的影响,实验结果可表示成如图所示的规律(T表示温度,n表示物质的量):
某科研小组研究在其他条件不变的情况下,改变起始氢气物质的量[用n(H2)表示]对N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol 反应的影响,实验结果可表示成如图所示的规律(T表示温度,n表示物质的量):