题目内容
1.对复杂的有机物的结构,可以用“键线式”简化表示.如有机物CH2=CH一CHO可以简写成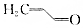 .则与键线式为
.则与键线式为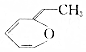 的物质互为同分异构体的是( )
的物质互为同分异构体的是( )| A. |  | B. |  | C. | 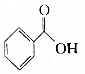 | D. | 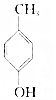 |
分析 同分异构体的分子式相同,但结构不同, 的分子式为C7H8O,以此来分析.
的分子式为C7H8O,以此来分析.
解答 解:A. 的分子式为C8H10O,与
的分子式为C8H10O,与 的分子式不同,不是同分异构体,故A不选;
的分子式不同,不是同分异构体,故A不选;
B. 的分子式为C7H6O,与
的分子式为C7H6O,与 的分子式不同,不是同分异构体,故B不选;
的分子式不同,不是同分异构体,故B不选;
C. 的分子式为C7H6O2,与
的分子式为C7H6O2,与 的分子式不同,不是同分异构体,故C不选;
的分子式不同,不是同分异构体,故C不选;
D. 与
与 的分子式均为C7H8O,但结构不同,互为同分异构体,故D选;
的分子式均为C7H8O,但结构不同,互为同分异构体,故D选;
故选D.
点评 本题考查有机物的结构及同分异构体,明确碳形成四个化学键确定有机物的分子式是解答本题的关键,注意同分异构体概念的理解,题目难度不大.

练习册系列答案
相关题目
13.研究和解决二氧化碳捕集和转化问题是当前科学研究的前沿领域.自然界中碳循环如图所示:

(1)在海洋中化石燃料转化为地质碳酸盐的过程中发生的反应类型有化合反应或氧化反应或裂解反应.
(2)光合作用是把无机物转化为有机物的同时,还能把光能转化为化学能.
(3)化石燃料最终转化为CO2,要使化石燃料充分燃烧,需测定煤或石油中的含碳量:将a g的样品进行充分燃烧,测定所得气体 ( CO2、SO2、NO2、N2、O2 ) 中CO2的含量.实验装置如图1所示 ( 所用试剂均过量 ):
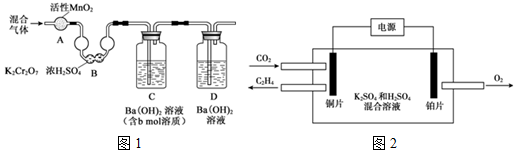
①混合气体通过A和B的目的是除去SO2、NO2,防止对Ba(OH)2吸收CO2造成干扰
②装置D的作用是防止空气中的CO2进入装置C,造成测碳量产生误差
③实验结束后,还需要向装置中通入N2,其目的是将装置A、B中的气体赶入装置C中,确保CO2被完全吸收.
④用x mol/L HCl溶液滴定装置C中过量的Ba(OH)2,消耗y mLHCl溶液,a g样品中碳元素的质量分数为$\frac{(b-\frac{1}{2}xy×1{0}^{-3})×12}{a}$×100%(列出计算式).
(4)用稀氨水喷雾捕集CO2最终可得产品NH4HCO3.在捕集时,气相中有中间体 NH2COONH4(氨基甲酸铵)生成.现将一定量纯净的氨基甲酸铵置于恒容的密闭真空容器中,分别在不同温度下进行反应:NH2COONH4(s)?2NH3(g)+CO2(g).实验测得的有关数据见表. ( t1 <t2 <t3 )
①在15℃,用 NH3 的浓度变化表示 0~t1 时间段的反应速率为:$\frac{6×1{0}^{-3}}{{t}_{1}}$mol/(L•min)
②能证明该反应在t2时刻达到化学平衡的是a c(选填字母).
a.容器内压强不再变化 b.容器内 NH3、CO2物质的量比为 2:1
c.容器内气体的质量不再变化 d.生成CO2的速率与消耗NH3速率相等
(5)用一种钾盐的酸性水溶液作电解质,CO2电催化还原为碳氢化合物(其原理见图2).铂电极是阳(填“阴”或“阳”)极;在铜极上产生乙烯的电极反应式是2CO2+12H++12e -═C2H4+4H2O.

(1)在海洋中化石燃料转化为地质碳酸盐的过程中发生的反应类型有化合反应或氧化反应或裂解反应.
(2)光合作用是把无机物转化为有机物的同时,还能把光能转化为化学能.
(3)化石燃料最终转化为CO2,要使化石燃料充分燃烧,需测定煤或石油中的含碳量:将a g的样品进行充分燃烧,测定所得气体 ( CO2、SO2、NO2、N2、O2 ) 中CO2的含量.实验装置如图1所示 ( 所用试剂均过量 ):

①混合气体通过A和B的目的是除去SO2、NO2,防止对Ba(OH)2吸收CO2造成干扰
②装置D的作用是防止空气中的CO2进入装置C,造成测碳量产生误差
③实验结束后,还需要向装置中通入N2,其目的是将装置A、B中的气体赶入装置C中,确保CO2被完全吸收.
④用x mol/L HCl溶液滴定装置C中过量的Ba(OH)2,消耗y mLHCl溶液,a g样品中碳元素的质量分数为$\frac{(b-\frac{1}{2}xy×1{0}^{-3})×12}{a}$×100%(列出计算式).
(4)用稀氨水喷雾捕集CO2最终可得产品NH4HCO3.在捕集时,气相中有中间体 NH2COONH4(氨基甲酸铵)生成.现将一定量纯净的氨基甲酸铵置于恒容的密闭真空容器中,分别在不同温度下进行反应:NH2COONH4(s)?2NH3(g)+CO2(g).实验测得的有关数据见表. ( t1 <t2 <t3 )
| 温度(℃) CO2 浓度 (mol/L) 时间(min) | 15 | 25 | 35 |
| 0 | 0 | 0 | 0 |
| t1 | 3×10-3 | 0.9×10-2 | 2.7×10-2 |
| t2 | 1×10-3 | 1.6×10-2 | 3.1×10-2 |
| t3 | 1×10-3 | 1.6×10-2 | 3.1×10-2 |
②能证明该反应在t2时刻达到化学平衡的是a c(选填字母).
a.容器内压强不再变化 b.容器内 NH3、CO2物质的量比为 2:1
c.容器内气体的质量不再变化 d.生成CO2的速率与消耗NH3速率相等
(5)用一种钾盐的酸性水溶液作电解质,CO2电催化还原为碳氢化合物(其原理见图2).铂电极是阳(填“阴”或“阳”)极;在铜极上产生乙烯的电极反应式是2CO2+12H++12e -═C2H4+4H2O.
16.已知c(NH4Cl)≤0.1mol/L时,溶液pH>5.1.现用0.1mol/L盐酸滴定10mL 0.05mol/L氨水,用甲基橙作指示剂,达到滴定终点,所用盐酸的体积为( )
| A. | 10 mL | B. | 5 mL | C. | 大于5 mL | D. | 小于5 mL |
13.关于容量瓶的使用,下列操作正确的是( )
| A. | 使用前要先检查容量瓶是否漏液 | |
| B. | 用蒸馏水洗涤后必须要将容量瓶烘干 | |
| C. | 为了方便快捷,可以直接在容量瓶内进行固体溶解 | |
| D. | 定容结束后,为了使溶液均匀,手握瓶颈,左右振荡 |
10.下列物质中,不能由金属与非金属直接化合生成的是( )
| A. | FeCl2 | B. | FeCl3 | C. | Na2S | D. | Fe3O4 |
11.下列有关物质用途的说法中,不正确的是( )
| A. | SO2可用于漂白纸浆 | B. | SiO2是良好的半导体材料 | ||
| C. | Na2O2可用作潜水艇O2来源 | D. | Cl2可用于消毒和制造漂白粉 |
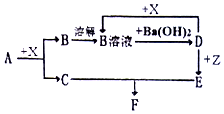 下列物质均为常见物质或它们的溶液,其中A为淡黄色固休,C、X均为无色气体,Z为浅绿色溶液,D为一种常见的强碱.根据它们之间的转化关系(如图),用化学用语回答问题.(部分产物已省略)
下列物质均为常见物质或它们的溶液,其中A为淡黄色固休,C、X均为无色气体,Z为浅绿色溶液,D为一种常见的强碱.根据它们之间的转化关系(如图),用化学用语回答问题.(部分产物已省略) .
.