题目内容
9.简要回答下列问题.(1)铝制器具不宜存放酸、碱溶液的原因是金属铝可以和酸、碱之间反应.
(2)实验室常用35%~40%的甲醛溶液(俗称福尔马林)保存动物标本的原因是甲醛能使蛋白质变性.
(3)可降解塑料在环境中可以降解为小分子物质或被微生物分解.研制生产可降解塑料的目的是减少白色污染.
分析 (1)金属铝可以和酸、碱之间反应,据此回答;
(2)甲醛能使蛋白质变性,用来保存保存动物标本;
(3)根据塑料能形成白色污染来回答.
解答 解:(1)金属铝可以和酸、碱之间反应,铝制器具不宜存放酸、碱溶液,故答案为:金属铝可以和酸、碱之间反应;
(2)甲醛能使蛋白质变性,实验室常用35%~40%的甲醛溶液(俗称福尔马林)保存动物标本,故答案为:甲醛能使蛋白质变性;
(3)塑料能形成白色污染,所以研制生产可降解塑料代替塑料可以减少白色污染,故答案为:减少白色污染.
点评 本题考查了化学知识在生产、生活中的应用,侧重于基础知识的考查,题目难度不大.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
20.草酸是二元中强酸,草酸氢钠溶液显酸性.常温下,向10mL 0.01mol/L NaHC2O4溶液中滴加0.01mol/L NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是( )
| A. | V(NaOH)=0时,c(H+)=1×10-2 mol/L | |
| B. | V(NaOH)=10 mL时,c(H+)=1×10-7 mol/L | |
| C. | V(NaOH)<10 mL时,可能存在c(Na+)=2c(C2O42-)+c(HC2O4-) | |
| D. | V(NaOH)>10 mL时,2c(C2O42-)>c(Na+)>c(HC2O4-) |
17.海水浓缩的过程中,随着水分的蒸发,当海水密度达到1.13g/mL时,首先析出的化学物质是( )
| A. | 氯化钠 | B. | 硫酸钙 | C. | 硫酸镁 | D. | 氯化镁 |
4.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 含NA个阴离子的Na2O2溶于水形成1L溶液,其物质的量的浓度为1mol/L | |
| B. | 25g质量分数为68%的H2O2水溶液中含有氧原子数目为NA | |
| C. | 常温常压下,0.1molD2O含有中子数为NA | |
| D. | 用5mL3mol/LFeCl3溶液制成的氢氧化铁胶体中所含胶粒数为0.015 NA |
14.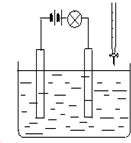 在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )
在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )
 在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )
在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )| A. | 盐酸中逐滴加入食盐溶液 | B. | 硫酸中逐滴加入氢氧化钠溶液 | ||
| C. | 硫酸中逐滴加入氢氧化钡溶液 | D. | 醋酸中逐渐加入氢氧化钠溶液 |
1.一种充电电池放电时的电极反应为H2+2OH--2e-═2H2O; NiO(OH)+H2O+e-═Ni(OH)2+OH-
当为电池充电时,与外电源正极连接的电极上发生的反应是( )
当为电池充电时,与外电源正极连接的电极上发生的反应是( )
| A. | NiO(OH) 2的氧化 | B. | NiO(OH)的还原 | C. | H2O的氧化 | D. | H2O的还原 |
18.向60mLNa2SO4溶液中加入BaCl2溶液,有关数据见表:
下列有关说法正确的是( )
| 实验编号 | 1 | 2 | 3 | 4 | 5 |
| BaCl2溶液体积/mL | 0 | 20 | 40 | 100 | 120 |
| 沉淀质量/g | 0 | 0.233 | m | 0.699 | 0.699 |
| A. | 混合前,Na2SO4溶液的物质的量浓度为0.05mol/L | |
| B. | 混合前,BaCl2溶液的物质的量浓度为0.10mol/L | |
| C. | 3号实验中沉淀的质量m为0.398g | |
| D. | 完全沉淀60mLNa2SO4溶液消耗BaCl2溶液的体积为80mL |
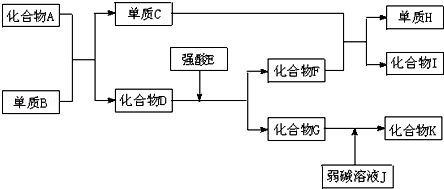
17.氯化锶晶体在工业上常用作铝的缓蚀剂.工业上一般用难溶于水的碳酸锶(SrCO3)为原料(含少量钡和铁的化合物等),制备高纯六水氯化锶晶体(SrCl2•6H2O)的过程为:

已知:Ⅰ.SrCl2•6H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水.
Ⅱ.有关氢氧化物开始沉淀和完全沉淀的pH如表:
(1)操作①在实际工业生产中常常把碳酸锶粉碎并加以搅拌,其目的是加快反应速率.碳酸锶与盐酸反应的化学方程式为SrCO3+2HCl=SrCl2+CO2↑+H2O.
(2)酸性条件下,加入30% H2O2溶液,将Fe2+氧化成Fe3+,其离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.能否用新制氯水代替双氧水能(填“能”或“否”).
(3)在步骤②-③的过程中,将溶液的pH值由1调节至B;宜用的试剂为EG.
A.1.5 B.4 C.9.7
D.氨水 E.氢氧化锶粉末 F.碳酸钠晶体 G.氧化锶粉末
(4)操作③中所得滤渣的主要成分是Fe(OH)3、BaSO4(填化学式).
(5)工业上用50~60℃热风吹干六水氯化锶,选择该温度的原因是温度高有利于除去湿存(晶体表面附着的)水,但温度高于61℃时,氯化锶晶体中的结晶水也会失去.
(6)步骤⑥中,洗涤氯化锶晶体最好选用D.
A.水 B.稀硫酸 C.氢氧化钠溶液 D.氯化锶饱和溶液.

已知:Ⅰ.SrCl2•6H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水.
Ⅱ.有关氢氧化物开始沉淀和完全沉淀的pH如表:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 |
| 沉淀完全的pH | 3.7 | 9.7 |
(2)酸性条件下,加入30% H2O2溶液,将Fe2+氧化成Fe3+,其离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.能否用新制氯水代替双氧水能(填“能”或“否”).
(3)在步骤②-③的过程中,将溶液的pH值由1调节至B;宜用的试剂为EG.
A.1.5 B.4 C.9.7
D.氨水 E.氢氧化锶粉末 F.碳酸钠晶体 G.氧化锶粉末
(4)操作③中所得滤渣的主要成分是Fe(OH)3、BaSO4(填化学式).
(5)工业上用50~60℃热风吹干六水氯化锶,选择该温度的原因是温度高有利于除去湿存(晶体表面附着的)水,但温度高于61℃时,氯化锶晶体中的结晶水也会失去.
(6)步骤⑥中,洗涤氯化锶晶体最好选用D.
A.水 B.稀硫酸 C.氢氧化钠溶液 D.氯化锶饱和溶液.
 .
.