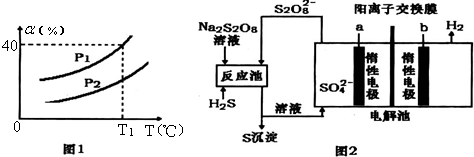
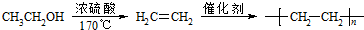题目内容
3.如表各组物质中,可以实现X$\stackrel{M}{→}$Y$\stackrel{M}{→}$Z(每步只发生一个反应)所示转化的选项是( )| 选项 | X | Y | Z | M |
| A | Fe | FeCl2 | FeCl3 | Cl2 |
| B | C | CO | CO2 | O2 |
| C | CO2 | Na2CO3 | NaHCO3 | NaOH |
| D | AlO2- | Al(OH)3 | Al3+ | CO2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Fe与氯气反应生成氯化铁,不能生成氯化亚铁;
B.过量的碳与氧气反应生成CO,CO与氧气反应生成二氧化碳,符合转化关系;
C.碳酸钠不能与氢氧化钠反应;
D.氢氧化铝溶于强酸,但不能溶于碳酸.
解答 解:A.Fe与氯气反应生成氯化铁,不能生成氯化亚铁,不符合转化关系,故A错误;
B.过量的碳与氧气反应生成CO,CO在氧气中燃烧生成二氧化碳,符合转化关系,故B正确;
C.二氧化碳与氢氧化钠反应生成碳酸钠,但碳酸钠不能与氢氧化钠反应,不符合转化关系,故C错误;
D.溶液中四羟基合铝酸根能与二氧化碳反应生成氢氧化铝沉淀,氢氧化铝溶于强酸,但不能溶于弱酸碳酸,不符合转化关系,故D错误,
故选B.
点评 本题考查元素化合物性质,明确物质的性质是解本题关键,注意铁在氯气中燃烧,无论铁是否过量都生成氯化铁,注意掌握常见反应物相同,反应条件不同、反应物的量不同、滴加顺序不同,导致产物不同.

练习册系列答案
相关题目
13.在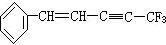 分子中,位于同一平面上的原子数最多可能是( )
分子中,位于同一平面上的原子数最多可能是( )
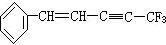 分子中,位于同一平面上的原子数最多可能是( )
分子中,位于同一平面上的原子数最多可能是( )| A. | 17 个 | B. | 18 个 | C. | 19 个 | D. | 20 个 |
14.有a、b、c、d四种元素,原子序数依次增大.a存在a+和a-两种离子,b和c为短周期同一主族元素,c的次外层有8个电子,c2-和d2+的电子层结构相同.下列叙述正确的是( )
| A. | b和c分别与a形成化合物的相对分子质量一定为b>c | |
| B. | a和d形成的化合物与水反应产生的气体可做燃料 | |
| C. | +6价的c和a、b形成离子化合物 | |
| D. | a、b、c和d四种元素组成的化合物的水溶液加入少量Na2CO3只产生气体,不产生沉淀 |
18.CO分析仪以燃料电池为工作原理,用来测量汽车尾气中的CO的含量,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法错误的是( )
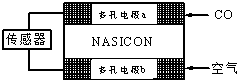

| A. | 负极的电极反应式为:CO+O2--2e-═CO2 | |
| B. | 工作时电极b作正极,O2-由电极a流向电极b | |
| C. | 工作时电子由电极a通过传感器流向电极b | |
| D. | 传感器中通过的电流越大,尾气中CO的含量越高 |
8.下列物质性质与应用对应关系正确的是( )
| A. | 火碱能与酸反应,可用于治疗胃酸过多 | |
| B. | 晶体硅硬度大,可用于制作半导体材料 | |
| C. | SO2具有还原性,可用于漂白纸浆 | |
| D. | MgO、Al2O3熔点高,它们都可用于制作耐火材料 |
12.X、Y、Z、W、M均为短周期元素,X、Y处于同一周期,Z、W处于同一周期,X、Y 原子最外层电子数之和等于Z、W 原子最外层电子数之和,Y 是形成化合物种类最多的元素,X、W 的简单离子X2-、W3+具有相同的电子层结构,M为短周期中除稀有气体元素外原子半径最大的元素.下列说法正确的是( )
| A. | X最高价氧化物对应的水化物为强酸 | |
| B. | 原子半径大小顺序为M>W>X>Y>Z | |
| C. | 水溶液中Z 的简单单核离子能促进水的电离 | |
| D. | Z、M的最高价氧化物对应的水化物均能溶解W与X形成的化合物 |
13.如表叙述不正确的是( )
| A | B | C | D |
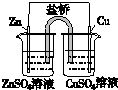 | 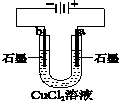 |  |  |
| 盐桥中的Cl-移向ZnSO4溶液 | a极附近产生的气体能使湿润的淀粉碘化钾试纸变蓝 | 粗铜的电极反应式为:Cu2++2e-=Cu | 正极反应式为: O2+4e-+2H2O=4OH- |
| A. | A | B. | B | C. | C | D. | D |
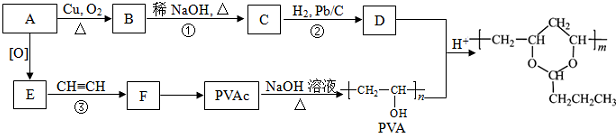
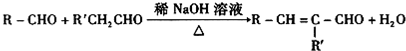
 (R、R′可表示烃基或氢原子)
(R、R′可表示烃基或氢原子)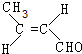 ,该分子中最多有9个原子共平面.
,该分子中最多有9个原子共平面. $→_{△}^{NaOH}$
$→_{△}^{NaOH}$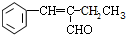 +H2O.
+H2O.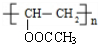 .
. .合成路线流程图示例如下:
.合成路线流程图示例如下: