题目内容
18.CO分析仪以燃料电池为工作原理,用来测量汽车尾气中的CO的含量,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法错误的是( )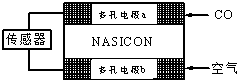
| A. | 负极的电极反应式为:CO+O2--2e-═CO2 | |
| B. | 工作时电极b作正极,O2-由电极a流向电极b | |
| C. | 工作时电子由电极a通过传感器流向电极b | |
| D. | 传感器中通过的电流越大,尾气中CO的含量越高 |
分析 该装置属于原电池,一氧化碳失电子发生氧化反应生成二氧化碳,则通入一氧化碳的电极为负极,正极上氧气得电子发生还原反应,原电池放电时电子从负极流向正极,阴离子向负极移动,一氧化碳的含量越大,原电池放电时产生的电流越大.
解答 解:A.负极上一氧化碳失电子和氧离子反应生成二氧化碳,电极反应式为CO+O2--2e-=CO2,故A正确;
B.原电池放电时,阴离子向负极移动,该原电池中,a是负极,b是正极,所以氧离子由b电极向a电极移动,故B错误;
C.放电时,a作负极,b作正极,电子从负极a通过传感器流向电极b,故C正确;
D.一氧化碳的含量越大,一氧化碳失电子越多,则原电池放电时产生的电流越大,故D正确;
故选:B.
点评 本题是对CO-O2型燃料电池原理的考查,根据原电池正负极上得失电子及反应类型、离子的移动方向等来分析解答,注意电解质特点,难度不大.

练习册系列答案
相关题目
6.中国传统文化对人类文明贡献巨大,古代文献中充分记载了古代化学研究成果.《本草经集注》中写到“以火烧之,紫青烟起,乃真硝石也”.“硝石”指的是( )
| A. | Na2SO4 | B. | KNO3 | C. | Ca(NO3)2 | D. | KIO3 |
13.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 4.6g由NO2和N2O4组成的混合物中氧原子总数为0.2NA | |
| B. | 标准状况下,22.4L的SO3中含3NA个氧原子 | |
| C. | 100mL18.4mol/L的浓硫酸与足量的铜加热反应,转移的电子数为1.84NA | |
| D. | 密闭的容器中,催化剂作用下0.5molN2与1.5molH2反应后得到NH3分子数一定为NA |
3.如表各组物质中,可以实现X$\stackrel{M}{→}$Y$\stackrel{M}{→}$Z(每步只发生一个反应)所示转化的选项是( )
| 选项 | X | Y | Z | M |
| A | Fe | FeCl2 | FeCl3 | Cl2 |
| B | C | CO | CO2 | O2 |
| C | CO2 | Na2CO3 | NaHCO3 | NaOH |
| D | AlO2- | Al(OH)3 | Al3+ | CO2 |
| A. | A | B. | B | C. | C | D. | D |
10.在由水电离的c(H+)=10-12mol/L的溶液中,下列离子组一定能大量共存的是( )
| A. | Na+、K+、Cl?、NO3? | B. | K+、Na+、ClO?、SO42- | ||
| C. | Al3+、Cu2+、Cl?、S2- | D. | Na+、Fe2+、NO3-、Cl- |
7.下列说法正确的是( )
| A. | 红宝石、玛瑙、水晶、钻石等装饰品的主要成分都不相同 | |
| B. | 将Al2(SO4)3溶液蒸干、灼烧至恒重,最终剩余固体是Al2O3 | |
| C. | 白磷、臭氧、碳-60、氩、水等物质都是由分子构成的,分子内都存在共价键 | |
| D. | 工业生产玻璃、水泥、漂白粉,均需要用石灰石为原料 |
8.100mL 1mol•L-1的Ca(HCO3)2溶液中,放入2.3g金属钠充分反应后,有关物质的物理量正确的是(NA表示阿伏加德罗常数)( )
| 生成CaCO3 | 溶液中HCO3- | H2 | 转移的电子 | |
| A | 0.1NA | 0.1NA | ||
| B | 1.12L | 0.1NA | ||
| C | 10g | 0.05NA | ||
| D | 10g | 0.1NA |
| A. | A | B. | B | C. | C | D. | D |
 有如图所示某有机物,根据该有机物的结构回答:
有如图所示某有机物,根据该有机物的结构回答: .
.