题目内容
在一定温度下,向容积固定的密闭容器中充入amolC(g),发生如下可逆反应:2A(g)+B(g)?2C(g)△H<0.达平衡后再向容器中充入amolC(g),再达平衡后,与原平衡比较,下列叙述正确的是( )
| A、平均相对分子质量减小 |
| B、C的转化率增大 |
| C、C的质量分数增大 |
| D、反应热大于原来的2倍 |
考点:化学平衡建立的过程
专题:
分析:平衡后再向容器中充入amolC(g),可以假设成在另外一个与原容器一样大的容器中先建立一个与原平衡一样的平衡,再将这个容器中的气体加入原容器中,相当于对原容器加压,由于反应为气体体积减小的反应,所以平衡正向移动,再根据平衡移动对体系相关的影响,作判断;
解答:
解:平衡后再向容器中充入amolC(g),可以假设成在另外一个与原容器一样大的容器中先建立一个与原平衡一样的平衡,再将这个容器中的气体加入原容器中,相当于对原容器加压,由于反应为气体体积减小的反应,所以平衡正向移动,
A、因为反应前后气体总质量不变,为原来的2倍,平衡正向移动,总物质的量小于原来的2倍,所以平均相对分子质量增大,故A错误;
B、平衡正向移动,C的转化率减小,故B错误;
C、平衡正向移动,C的质量分数增大,故C正确;
D、在反应2A(g)+B(g)?2C(g)中的反应热是指2molA完全反应放出的热量,不随着C的量改变而改变,故D错误;
故选C.
A、因为反应前后气体总质量不变,为原来的2倍,平衡正向移动,总物质的量小于原来的2倍,所以平均相对分子质量增大,故A错误;
B、平衡正向移动,C的转化率减小,故B错误;
C、平衡正向移动,C的质量分数增大,故C正确;
D、在反应2A(g)+B(g)?2C(g)中的反应热是指2molA完全反应放出的热量,不随着C的量改变而改变,故D错误;
故选C.
点评:本题主要考查平衡移动后各物质的相关物理量的变化,中等难度,解题关键在于正确运用等效平衡的思想分析问题.

练习册系列答案
相关题目
下列关于化学反应限度的说法正确的是( )
| A、改变外界条件不能改变化学反应的限度 |
| B、当某反应在一定条件下达到反应限度时即达到了化学平衡状态 |
| C、当某反应达到限度时,反应物的浓度和生成物的浓度一定相等 |
| D、对于吸热反应,升高温度能增大正反应速率,降低逆反应速率 |
将固体NH4I置于密闭容器中,在某温度下发生下列可逆反应:NH4I(s)?NH3(g)+HI(g),
2HI(g)?H2(g)+I2(g);当反应达到平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则c(NH3)是( )
2HI(g)?H2(g)+I2(g);当反应达到平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则c(NH3)是( )
| A、5 mol/L |
| B、4.5 mol/L |
| C、4 mol/L |
| D、3.5 mol/L |
一定量的Mg和MgO的混合物投入到100mL 4mol?L-1H2SO4中完全溶解,再向反应后的溶液中加入4mol?L-1 NaOH溶液,要使反应后的Mg2+全部沉淀出来,加入的NaOH溶液的体积至少是( )
| A、100 mL |
| B、50 mL |
| C、200 mL |
| D、缺少数据,无法计算 |
下列图示操作正确的是( )
A、 为稀释浓硫酸 |
B、 为滴定前除去碱式滴定管尖嘴处气泡 |
C、 为向试管中加固体粉末状药品 |
D、 为向容量瓶中加水 |
用电解熔融氯化镁而不用电解氧化镁的方法制金属镁,可能的原因是( )
| A、易制得氯化镁,不易制得氧化镁 |
| B、溶融氧化镁不能被电解 |
| C、氧化镁熔点比氯化镁熔高得多 |
| D、氯化镁易溶于水,氧化镁不溶于水 |
有Na2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的物质的量浓度为0.4mol/L,SO42-的物质的量浓度为0.7mol/L,则此溶液中Na+的物质的量浓度为( )
| A、0.1 mol/L |
| B、0.15 mol/L |
| C、0.2 mol/L |
| D、0.25 mol/L |
下列实验方案设计合理且能达到相应实验预期目的是( )
A、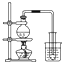 制取少量蒸馏水 |
B、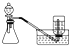 用铜和浓硝酸制取少量NO2 |
C、 证明氧化性:Cl2>Br2>I2 |
D、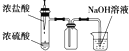 制取HCl且除去多余的气体 |
金属钠通常保存在( )
| A、水中 | B、煤油中 |
| C、汽油中 | D、四氯化碳中 |