题目内容
对于可逆反应A(g)+2B(g)?2C(g);△H>0,下列各图正确的是( )
A、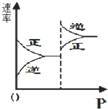 |
B、 |
C、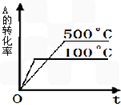 |
D、 |
考点:化学平衡建立的过程
专题:化学平衡专题
分析:A、对于有气体参加的反应,随着压强增大,反应速率不断增大,据此判断;
B、对于有气体参加的反应,增大压强,正逆反应速率都增大,据此判断;
C、温度越高,反应速率越大,图曲线起始的斜率就越大,据此判断;
D、该反应为吸热反应,升高温度平衡正向移动,A的百分含量下降,据此判断;
B、对于有气体参加的反应,增大压强,正逆反应速率都增大,据此判断;
C、温度越高,反应速率越大,图曲线起始的斜率就越大,据此判断;
D、该反应为吸热反应,升高温度平衡正向移动,A的百分含量下降,据此判断;
解答:
解:A、对于有气体参加的反应,随着压强增大,反应速率不断增大,故A错误;
B、对于有气体参加的反应,增大压强,正逆反应速率都增大,故B错误;
C、温度越高,反应速率越大,图曲线起始的斜率就越大,故C错误;
D、该反应为吸热反应,升高温度平衡正向移动,A的百分含量下降,故D正确;
故选D.
B、对于有气体参加的反应,增大压强,正逆反应速率都增大,故B错误;
C、温度越高,反应速率越大,图曲线起始的斜率就越大,故C错误;
D、该反应为吸热反应,升高温度平衡正向移动,A的百分含量下降,故D正确;
故选D.
点评:本题主要考查了影响化学反应速率的因素和影响平衡移动的因素,难度不大,解题时要注意图象的识别.

练习册系列答案
相关题目
将固体NH4I置于密闭容器中,在某温度下发生下列可逆反应:NH4I(s)?NH3(g)+HI(g),
2HI(g)?H2(g)+I2(g);当反应达到平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则c(NH3)是( )
2HI(g)?H2(g)+I2(g);当反应达到平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则c(NH3)是( )
| A、5 mol/L |
| B、4.5 mol/L |
| C、4 mol/L |
| D、3.5 mol/L |
有Na2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的物质的量浓度为0.4mol/L,SO42-的物质的量浓度为0.7mol/L,则此溶液中Na+的物质的量浓度为( )
| A、0.1 mol/L |
| B、0.15 mol/L |
| C、0.2 mol/L |
| D、0.25 mol/L |
下列实验方案设计合理且能达到相应实验预期目的是( )
A、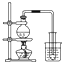 制取少量蒸馏水 |
B、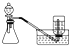 用铜和浓硝酸制取少量NO2 |
C、 证明氧化性:Cl2>Br2>I2 |
D、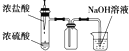 制取HCl且除去多余的气体 |
发射“嫦娥一号”月球探测卫星的长征三号甲运载火箭的第三子级使用的燃料是液氢和液氧,已知下列热化学方程式:
①H2(g)+
O2(g)=H2O(l)△H1=-285.8kJ/mol
②H2(g)=H2(l)△H2=-0.92kJ/mol
③O2(g)=O2(l)△H3=-6.84kJ/mol
④H2O(l)=H2O(g)△H4=+44.0kJ/mol
则反应H2(l)+
O2(l)=H2O(g)的反应热△H为( )
①H2(g)+
| 1 |
| 2 |
②H2(g)=H2(l)△H2=-0.92kJ/mol
③O2(g)=O2(l)△H3=-6.84kJ/mol
④H2O(l)=H2O(g)△H4=+44.0kJ/mol
则反应H2(l)+
| 1 |
| 2 |
| A、+237.46 kJ/mol |
| B、-474.92 kJ/mol |
| C、-118.73 kJ/mol |
| D、-237.46 kJ/mol |
除去二氧化碳中混有的少量二氧化硫气体,可选用的试剂是( )
| A、饱和食盐水 |
| B、NaOH溶液 |
| C、足量澄清石灰水 |
| D、饱和碳酸氢钠溶液 |
相同状况下,n mol氢气和n mol二氧化碳的体积相同,下列解释错误的是( )
| A、n mol氢气和n mol二氧化碳所含的气体分子数目相同 |
| B、相同状况下,氢分子间的平均距离和二氧化碳分子间的平均距离大致相等 |
| C、氢分子本身的大小和二氧化碳分子本身的大小大致相同 |
| D、气体分子本身大小相对分子间平均距离来说可忽略不计 |
金属钠通常保存在( )
| A、水中 | B、煤油中 |
| C、汽油中 | D、四氯化碳中 |