题目内容
下列说法不正确的是( )
| A、离子反应的活化能几乎为零 |
| B、发生有效碰撞的分子一定是活化分子 |
| C、活化能对化学反应的反应热会产生影响 |
| D、活化能指活化分子多出其它反应物分子的那部分能量 |
考点:活化能及其对化学反应速率的影响
专题:
分析:A、在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能;
B、根据化学反应历程,发生有效碰撞的分子一定是活化分子;
C、活化能越大,反应越难以进行,但反应热和活化能无关;
D、使普通分子变成活化分子所需提供的最低限度的能量叫活化能.
B、根据化学反应历程,发生有效碰撞的分子一定是活化分子;
C、活化能越大,反应越难以进行,但反应热和活化能无关;
D、使普通分子变成活化分子所需提供的最低限度的能量叫活化能.
解答:
解:A、离子反应中,离子已是活化离子,故其活化能为零,故A正确;
B、由化学反应历程可知,发生有效碰撞的分子一定是活化分子,故B正确;
C、活化能越大,反应越难以进行,但反应热和活化能无关,只与反应物和生成物总能量有关,故C错误;
D、使普通分子变成活化分子所需提供的最低限度的能量叫活化能,即活化能指活化分子多出其它反应物分子的那部分能量,故D正确.
故选C.
B、由化学反应历程可知,发生有效碰撞的分子一定是活化分子,故B正确;
C、活化能越大,反应越难以进行,但反应热和活化能无关,只与反应物和生成物总能量有关,故C错误;
D、使普通分子变成活化分子所需提供的最低限度的能量叫活化能,即活化能指活化分子多出其它反应物分子的那部分能量,故D正确.
故选C.
点评:本题考查了活化能以及有效有效碰撞,侧重基础总是的考查,题目难度不大.

练习册系列答案
相关题目
下列有关生活生产中的叙述合理的是( )
| A、硫酸工业中SO2转化为SO3时采用常压,是因为增大压强不会提高SO2的转化率 |
| B、打开啤酒瓶的瓶盖,有大量的气泡冒出来,该现象不能用勒夏特列原理解释 |
| C、氯碱工业中用离子交换膜电解槽电解时,往阴极室注入经过精制的饱和NaCl溶液,往阳极室注入稀氢氧化钠溶液(或去离子水) |
| D、工业上合成氨采用500℃左右的温度,最主要原因是该反应的催化剂在500℃左右时活性最好 |
下列电池属于二次电池的是( )
 |  |  |  |
| A. 锌银钮扣电池 | B.氢氧燃料电池 | C.铅蓄电池 | D.锌锰干电池 |
| A、A | B、B | C、C | D、D |
下列叙述正确的是 ( )
| A、红热的铜丝在氯气中剧烈燃烧,生成棕黄色的烟,加少量的水形成绿色溶液 |
| B、检验氨气的方法是将湿润的蓝色石蕊试纸靠近瓶口或管口,观察试纸是否呈红色 |
| C、在淀粉溶液中加入稀硫酸并加热数分钟,冷却后依次加入新制Cu(OH)2悬浊液和碘水可检验淀粉是否已发生水解和是否完全水解 |
| D、铁钉放试管中,加入2mL水、3滴稀醋酸和1滴K3[Fe(CN)6]溶液,不久铁钉周围出现蓝色溶液 |
下列实验操作不能达到预期目的是( )
| A、用饱和NaHCO3溶液除去CO2中少量的HCl |
| B、NH4C1和I2的固体混合物可以用加热的方法分离 |
| C、植物油和水的混合物可以用分液的方法分离 |
| D、溴水中的溴单质可以用四氯化碳萃取 |
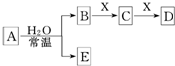 由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去),下列推断不正确的是( )
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去),下列推断不正确的是( )| A、若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐 |
| B、若D为CO,C能和E反应,则A是Na2O2,X的同素异形体只有3种 |
| C、若A是单质,B和D的反应是OH-+HCO3-=H2O+CO32-,则E一定能还原Fe2O3 |
| D、若X是Na2SO3,C为气体,则A可能是氯气,且D和E能发生反应 |
将足量的铜片与100 ml 18 mol?L-1浓硫酸加热充分反应,收集到标准状况下的SO2气体V L,下列对此反应的有关说法中错误的是 ( )
| A、该反应体现了浓硫酸的酸性和强氧化性 | ||
| B、应体结束后两两种反应物均有剩余 | ||
C、被还原的硫酸为
| ||
| D、参加反应的Cu为0.9 mol |