题目内容
下列对各组离子或物质是否能够大量共存及解释正确的是( )
| A | c(OH-)=1×10-13mol/L溶液中:Fe2+、NO3-、SO42-、Na+ | 不能共存 | 发生反应 3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O |
| B | 溶液中:K+、Cu2+、Cl-、NH3?H2O | 不能共存 | 发生反应Cu2++2OH-=Cu(OH)2↓ |
| C | 常温常压下:NH3、O2、H2、CO2 | 不能共存 | NH3为碱性气体,CO2为酸性气体,二者反应生成(NH4)2CO3 |
| D | 溶液中:Al3+、Na+、SO42-、HCO3- | 可以共存 | 不能发生反应 |
| A、A | B、B | C、C | D、D |
考点:离子共存问题
专题:
分析:A.c(OH-)=1×10-13mol/L溶液呈酸性,Fe2+、NO3-发生氧化还原反应;
B.Cu2+、NH3?H2O可发生络合反应;
C.氨气于二氧化碳在溶液中反应;
D.离子发生互促水解.
B.Cu2+、NH3?H2O可发生络合反应;
C.氨气于二氧化碳在溶液中反应;
D.离子发生互促水解.
解答:
解:A.c(OH-)=1×10-13mol/L溶液呈酸性,酸性条件下Fe2+、NO3-发生氧化还原反应:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,故A正确;
B.Cu2+、NH3?H2O可发生络合反应,应生成Cu(NH3?H2O)42+,故B错误;
C.氨气于二氧化碳在溶液中反应,干燥的氨气和二氧化碳不反应,可大量共存,故C错误;
D.Al3+、HCO3-发生互促水解,生成氢氧化铝沉淀和二氧化碳气体,不能大量共存,故D错误.
故选A.
B.Cu2+、NH3?H2O可发生络合反应,应生成Cu(NH3?H2O)42+,故B错误;
C.氨气于二氧化碳在溶液中反应,干燥的氨气和二氧化碳不反应,可大量共存,故C错误;
D.Al3+、HCO3-发生互促水解,生成氢氧化铝沉淀和二氧化碳气体,不能大量共存,故D错误.
故选A.
点评:本题考查了离子共存的判断,为高频考点,侧重学生的分析能力的考查,题目难度中等,注意熟练掌握离子反应发生的条件:生成气体、难溶物、沉淀及发生氧化还原反应.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
下列说法不正确的是( )
| A、离子反应的活化能几乎为零 |
| B、发生有效碰撞的分子一定是活化分子 |
| C、活化能对化学反应的反应热会产生影响 |
| D、活化能指活化分子多出其它反应物分子的那部分能量 |
下列作用不属于水解反应的是( )
| A、吃馒头时多咀嚼后有甜味 |
| B、淀粉溶液和稀硫酸共热一段时间后,滴加碘水不显蓝色 |
| C、葡萄糖被氧化成二氧化碳与水 |
| D、油脂与氢氧化钠溶液共煮后制肥皂 |
下列行为不会对环境造成污染的是( )
| A、将生活垃圾就地焚烧 |
| B、大量使用农药以防治病虫害 |
| C、大力提倡使用空调 |
| D、工业废水经处理后循环再用 |
能用于工业生产的是( )
| A、钠在氯气中燃烧制氯化钠 |
| B、二氧化锰和浓盐酸共热制氯气 |
| C、氯气与消石灰反应制漂白粉 |
| D、电解NaCl溶液制金属钠 |
下列的图示与对应的传述相符的是( )
A、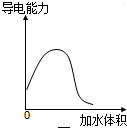 表示稀释冰醋酸过程中溶液导电性的变化曲线 |
B、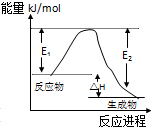 表示某一放热反应,若使用催化剂E1、E2,△H都会发生改变 |
C、 曲线表示将氢氧化钠滴加到醋酸溶液浓度的变化趋势 |
D、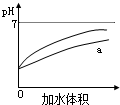 表示pH相同的盐酸与醋酸分别加入水中后溶液pH的变化,其中曲线a对应的是盐酸 |
工业上可利用反应2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4来制取ClO2,下列关于该反应的说法正确的是( )
| A、SO2发生还原反应 |
| B、NaClO3失去电子 |
| C、H2SO4作氧化剂 |
| D、1mol氧化剂得到1mol电子 |