题目内容
下列关于原电池的说法正确的是( )
| A、电流从原电池的负极流向正极 |
| B、电子从发生还原反应的电极流出 |
| C、原电池是将化学能转变为电能的一种装置 |
| D、原电池的两极,一定是由活动性不同的两种金属组成 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.电流从原电池正极流向负极;
B.电子从负极流出;
C.原电池放电过程中将化学能转化为电能;
D.原电池的两极,可能是由活动性不同的两种金属组成.
B.电子从负极流出;
C.原电池放电过程中将化学能转化为电能;
D.原电池的两极,可能是由活动性不同的两种金属组成.
解答:
解:A.原电池放电时,电流从原电池正极流向负极,电子流向与此相反,故A错误;
B.电子从负极流出,负极上失电子发生氧化反应,所以电子从发生氧化反应的电极流出,故B错误;
C.原电池放电过程中将化学能转化为电能,所以原电池是将化学能转化为电能的装置,故C正确;
D.原电池的两极,可能是由活动性不同的两种金属组成,也可能是由一种较活泼的金属和导电的非金属组成,故D错误;
故选C.
B.电子从负极流出,负极上失电子发生氧化反应,所以电子从发生氧化反应的电极流出,故B错误;
C.原电池放电过程中将化学能转化为电能,所以原电池是将化学能转化为电能的装置,故C正确;
D.原电池的两极,可能是由活动性不同的两种金属组成,也可能是由一种较活泼的金属和导电的非金属组成,故D错误;
故选C.
点评:本题考查了原电池原理,涉及原电池概念、电子和电流流向、电极材料等知识点,易错选项是D,注意原电池两个电极可能全部是非金属材料,如氢氧燃料电池中两个电极都是石墨,为易错点.

练习册系列答案
相关题目
下列关于电解质、非电解质的说法正确的是( )
| A、氯气溶于水得氯水,该溶液能导电,因此氯气是电解质 |
| B、CaCO3饱和溶液导电能力很弱,故CaCO3是弱电解质 |
| C、导电能力弱的溶液肯定是弱电解质的溶液 |
| D、HF的水溶液中既有H+、F-,又有大量的HF分子,因此HF是弱电解质 |
NA表示阿伏加德罗常数,下列判断正确的是( )
| A、含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol?L-1 |
| B、1L0.1mol?L-1的氨水含有0.1NA个NH3?H2O |
| C、5.6 g铁和6.4 g铜分别与0.1 mol氯气完全反应,转移的电子数相等 |
| D、10LpH=1的硫酸溶液中含有的H+离子数为2NA |
苯酚和苯甲醇共同的化学性质是( )
| A、酸性 |
| B、与钠反应放出氢气 |
| C、遇FeCl3溶液显紫色 |
| D、与NaOH溶液反应 |
下列化学式只能表示一种物质的是( )
| A、C4H8 |
| B、CH2Cl2 |
| C、C2H6O |
| D、C2H4O2 |
下列各组物质的性质变化正确的是( )
| A、酸性:HClO4>HNO3>H3PO4>H2SiO3 |
| B、稳定性:H2S>HCl>HBr>HI |
| C、熔点:Rb>K>Na>Li |
| D、溶解性:NaHCO3>Na2CO3>NaOH |
下列说法不正确的是( )
| A、铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 |
| C、一定条件下,使用催化剂能加快反应速率 |
| D、相同条件下,溶液中Fe3+、Cu2+、Zn2+的氧化性依次减弱 |
某化合物6.4g在氧气中完全燃烧,只生成8.8g CO2和7.2g H2O.下列说法正确的是( )
| A、该化合物仅含碳、氢两种元素 |
| B、该化合物中碳、氢原子个数比为1:4 |
| C、无法确定该化合物是否含有氧元素 |
| D、该化合物一定是C2H8O2 |
有机物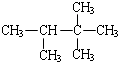 的名称是( )
的名称是( )
 的名称是( )
的名称是( )| A、2,3,3-三甲基丁烷 |
| B、2,3-三甲基丁烷 |
| C、2,2,3-三甲基丁烷 |
| D、2,3-三甲基丁烷 |