题目内容
11.阿伏加德罗常数的值为NA,下列说法中正确的是( )| A. | 56g铁粉在1mol氯气中充分燃烧,失去的电子数为3NA | |
| B. | 1mol 固体Na2O2含有的阴阳离子总数为3NA | |
| C. | 等体积、浓度均为1mol/L的磷酸和盐酸,电离出的氢离子数之比为3:1 | |
| D. | 1L 1 mol•L-1的NaClO 溶液中含有ClO-的数目为NA |
分析 A、56g铁饭即1mol铁粉在1mol氯气中燃烧,铁粉过量;
B、过氧化钠由2个钠离子和1个过氧根构成;
C、磷酸为中强酸,不能完全电离;
D、次氯酸根为弱酸根,在溶液中会水解.
解答 解:A、56g铁饭即1mol铁粉在1mol氯气中燃烧,铁粉过量,氯气完全反应,而由于氯气反应后变为-1价,故1mol氯气得2mol电子,则铁粉失去的电子为2mol,即为2NA个,故A错误;
B、过氧化钠由2个钠离子和1个过氧根构成,故1mol过氧化钠中含3mol离子即3NA个,故B正确;
C、磷酸为中强酸,不能完全电离,故两溶液中电离出的氢离子的个数之比小于3:1,故C错误;
D、次氯酸根为弱酸根,在溶液中会水解,故溶液中的次氯酸根的个数小于NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
1.你认为减少酸雨产生的途径可采取的措施是( )
①少用煤作燃料;②把工厂烟囱造高;③燃料脱硫;④在已酸化的土壤中加石灰;⑤开发新的能源.
①少用煤作燃料;②把工厂烟囱造高;③燃料脱硫;④在已酸化的土壤中加石灰;⑤开发新的能源.
| A. | ②③ | B. | ②③④⑤ | C. | ①③⑤ | D. | ①③④⑤ |
2.R为1~18号元素,其原子所具有的电子层数为最外层电子数的$\frac{1}{2}$,它可能形成的含氧酸根离子有:①RO32-,②RO42-,③R2O32-,下列叙述判断正确的是( )
| A. | 当它可以形成①时,不可能形成③ | B. | 当它形成①时,也可以形成②和③ | ||
| C. | 当它可以形成②时,不可能形成③ | D. | 当它可以形成①时,不可能形成② |
19.据报道,挪威和荷兰正在开发一种新能源--盐能.当海水和淡水混合时,温度将升高0.1℃,世界所有入海口的这种能源相当于电力需求的20%,海水和淡水混合时,温度升高最可能的原因是( )
| A. | 由于浓度差产生放热 | B. | 发生了水分解反应 | ||
| C. | 发生了盐分解反应 | D. | 盐的溶解程度增大 |
6.电解法制取有广泛用途的Na2FeO4,同时获得氢气.工作原理如图1所示,c( Na2FeO4)随初始c(NaOH)的变化如图2.
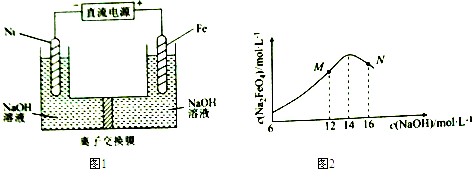
已知:FeO42-为紫红色;Na2FeO4只在强碱性条件下稳定,易被H2还原;溶液中OH-浓度过高,铁电极区会产生红褐色物质.下列说法错误的是( )

已知:FeO42-为紫红色;Na2FeO4只在强碱性条件下稳定,易被H2还原;溶液中OH-浓度过高,铁电极区会产生红褐色物质.下列说法错误的是( )
| A. | 制备Na2FeO4的电极反应为Fe-6e-+8OH-=FeO42-+4H2O | |
| B. | 电解过程中,须将阴极产生的气体及时排出 | |
| C. | MN两点中c(Na2FeO4)低于最高值的原因不同,在M点会有Fe(OH)3生成 | |
| D. | 图1中的离子交换膜为阴离子交换膜,电解过程中,阴极区附近pH会增大 |
16.硫酸亚铁(FeSO4)加热至高温会分解,生成一种金属氧化物M和两种非金属氧化物.某化学研究小组利用下列装置加热至高温使FeSO4分解.
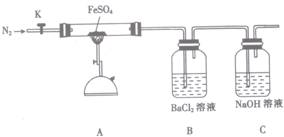
实验步骤:
将一定量FeSO4固体置于硬质玻璃管中,打开活塞K,通人一段时间N2,关闭活塞K.加热A中的玻璃管一段时间,待A中固体不再分解后,停止加热,打开K,缓慢通人氮气至玻璃管冷却.
(1)已知M中铁元素的质量分数为70%,M的化学式为Fe2O3.
(2)按图组装好仪器(已省略夹持仪器)并检查装置的气密性,在一定温度下按上述图示装置
进行实验.
(3)某同学欲验证硫酸亚铁分解产物中含有的另一种非金属氧化物N.
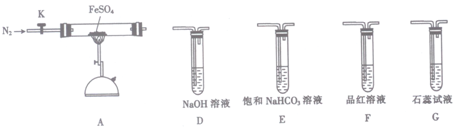
①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A→F→D.
②能证明生成了非金属氧化物N的现象是F中品红溶液褪色.

实验步骤:
将一定量FeSO4固体置于硬质玻璃管中,打开活塞K,通人一段时间N2,关闭活塞K.加热A中的玻璃管一段时间,待A中固体不再分解后,停止加热,打开K,缓慢通人氮气至玻璃管冷却.
(1)已知M中铁元素的质量分数为70%,M的化学式为Fe2O3.
(2)按图组装好仪器(已省略夹持仪器)并检查装置的气密性,在一定温度下按上述图示装置
进行实验.
| 操作步骤 | 实验现象 | 用化学方程式解释原因 |
| 打开K,通入一段时间的N2,关闭活塞K,加热A中的玻璃管一段时间 | 洗气瓶B中①有白色沉淀生成 | ②SO3+H2O+BaCl2=BaSO4↓+2HCl |
| A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却 | 硬质玻璃管中最终可以看到③有红棕色固体物质生成 | ④2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑ |

①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A→F→D.
②能证明生成了非金属氧化物N的现象是F中品红溶液褪色.
20.常温时,0.1mol/L HA溶液的pH>1,0.1mol/L BOH溶液中c(OH-):c(H+)=1012,将这两种溶液等体积混合,以下离子浓度关系判断正确的是( )
| A. | c(H+)<c(OH-)<c(B+)<c(A-) | B. | c(H+)<c(OH-)<c(A-)<c(B+) | ||
| C. | c(OH-)<c(H+)<c(B+)<c(A-) | D. | c(A-)=c(B+)>c(H+)=c(OH-) |
1.纯碱(Na2CO3)属于( )
| A. | 酸 | B. | 碱 | C. | 盐 | D. | 氧化物 |