题目内容
7.在一定温度下,向饱和烧碱溶液中投入一小块金属钠,充分反应后恢复到原来的温度,下列说法正确的是( )| A. | 溶液中Na+浓度增大,有H2放出 | |
| B. | 溶液中Na+数目减少,有H2放出 | |
| C. | 溶液中Na+与OH-浓度都增大,有H2放出 | |
| D. | 溶液中OH-数目增大,有H2放出 |
分析 依据钠和水反应生成氢氧化钠和氢气,反应消耗水,饱和的烧碱溶液中有NaOH析出解答.
解答 解:钠和水反应生成氢氧化钠和氢气,反应消耗水,饱和的烧碱溶液中有NaOH析出,所以所得溶液中钠离子和氢氧根离子的浓度不变,但因体积减少,导致钠离子和氢氧根离子的数目减少,
故选B.
点评 本题考查钠的性质,明确钠与水反应的实质是解题关键,注意饱和溶液的性质,溶剂减小,溶液中要析出晶体,但溶液的浓度不变,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,22.4 L水中所含原子总数为3NA | |
| B. | 常温常压下,44 gC3H8中含有的碳碳单键数为3NA | |
| C. | 标准状况下,44.8 L NO与22.4L O2混合后,气体分子总数为3NA | |
| D. | 1 molNa2O和Na2O2混合物中含有的阴.阳离子总数是3NA |
15.下列物质可用分液漏斗分离的是( )
| A. | 碘与酒精 | B. | 硝基苯与水 | C. | 苯与溴苯 | D. | 乙酸与水 |
2.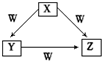 X、Y、Z、W是中学化学常见的四种物质,他们之间具有如图所示转化关系,则下列组合不可能的是( )
X、Y、Z、W是中学化学常见的四种物质,他们之间具有如图所示转化关系,则下列组合不可能的是( )
 X、Y、Z、W是中学化学常见的四种物质,他们之间具有如图所示转化关系,则下列组合不可能的是( )
X、Y、Z、W是中学化学常见的四种物质,他们之间具有如图所示转化关系,则下列组合不可能的是( )| X | Y | Z | W | |
| A | C | CO | CO2 | O2 |
| B | Na | Na2O | Na2O2 | O2 |
| C | AlCl3 | Al(OH)3 | NaAl(OH)4 | NaOH |
| D | Fe | FeCl2 | FeCl3 | Cl2 |
| A. | A | B. | B | C. | C | D. | D |
19.下列说法中不正确的是( )
| A. | 化学反应中的能量变化,通常表现为热量的变化 | |
| B. | 反应物的总能量高于生成物的总能量时发生放热反应 | |
| C. | Ba(OH)2•8H2O与NH4Cl的反应是吸热反应 | |
| D. | 一氧化碳在氧气中的燃烧是吸热反应 |
16.将一定量的Ag2SO4固体置于容积不变的容器中,在某温度下发生下列反应:
①Ag2SO4(s)?Ag2O(s)+SO3(g)
②2SO3(g)?2SO2(g)+O2(g)
经10分钟反应达到平衡,此时c(SO3)=0.4mol/L,c(O2)=0.05mol/L,下列叙述不正确的是( )
①Ag2SO4(s)?Ag2O(s)+SO3(g)
②2SO3(g)?2SO2(g)+O2(g)
经10分钟反应达到平衡,此时c(SO3)=0.4mol/L,c(O2)=0.05mol/L,下列叙述不正确的是( )
| A. | SO3的分解率为20% | B. | 10分钟内ν(SO2)=0.01mol/(L•min) | ||
| C. | 容器内气体的密度为40g/L | D. | 此温度下反应①的平衡常数为4 |
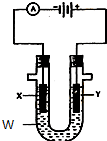 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液w;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液w;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: