题目内容
12.下列溶液中的各组离子能大量共存的是( )| A. | 含0.1 mol•L-1 CO32-的溶液中:Na+、K+、AlO2-、Cl- | |
| B. | 能与A1反应产生气泡的溶液中:Fe2+、Mg2+、I-、NO3-、 | |
| C. | 使酚酞变红的溶液中:NH4+、Al2+、Cl-、SO42- | |
| D. | 0.1 mol•L-1的盐酸中:Ca2+、K+、NO3-、HCO3- |
分析 A.四种离子之间不反应,能够不与碳酸根离子反应;
B.能与A1反应产生气泡的溶液中存在大量氢离子或氢氧根离子,亚铁离子、镁离子与氢氧根离子反应,酸性条件下硝酸根离子能够氧化亚铁离子和碘离子;
C.使酚酞变红的溶液中存在大量氢氧根离子,铵根离子、铝离子与氢氧根离子反应;
D.盐酸与碳酸氢根离子反应.
解答 解:A.Na+、K+、AlO2-、Cl-之间不反应,都不与CO32-反应,在溶液中能够大量共存,故A正确;
B.能与A1反应产生气泡的溶液呈酸性或碱性,Fe2+、Mg2+与氢氧根离子反应,酸性溶液中Fe2+、I-与NO3-发生氧化还原反应,在溶液中一定不能大量共存,故B错误;
C.使酚酞变红的溶液中存在大量氢氧根离子:NH4+、Al3+与氢氧根离子反应,在溶液中不能大量共存,故C错误;
D.HCO3-与盐酸反应生成二氧化碳气体和水,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的正误判断,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;试题侧重对学生基础知识的训练和检验,有利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
3.25℃时,关于指定溶液说法正确的是( )
| A. | pH=7的溶液中可能大量存在Fe3+、Cl-、Na+、S2- | |
| B. | 1 mol/L的FeCl3溶液滴入沸水中,得到分散质颗粒数为NA | |
| C. | 1 mol/L的Fe(NO3)2溶液中滴加盐酸,溶液变为黄色 | |
| D. | SO2与FeCl3溶液反应的离子方程式:2Fe3++SO2+4OH-=2Fe2++SO42-+2H2O |
20.化学与生产和生活密切相关.下列有关说法正确的是( )
| A. | 硅太阳能电池利用的是原电池原理 | B. | 草木灰与硝酸铵混成复合肥施用 | ||
| C. | 硅胶可用作瓶装药品的干燥剂 | D. | 用于发酵的小苏打属于碱 |
17.除去Cl2中混有的少量 HC1气体,可将气体通入( )
| A. | 饱和氯化钠溶液 | B. | 饱和碳酸氢钠溶液 | ||
| C. | 澄清石灰水 | D. | 氢氧化钠溶液 |
1.锂空气电池是一种新型的二次电池,其放电时的工作原理如图所示,下列说法正确的是( )
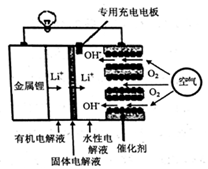

| A. | 正极区产生的LiOH可回收利用 | |
| B. | 电池中的有机电解液可以用稀盐酸代替 | |
| C. | 该电池放电时,正极的反应式为O2+4e-+4H+=2H2O | |
| D. | 该电池充电时,阴极发生了氧化反应:Li++e-=Li |
15.关于Cl-和Cl2的说法正确的是( )
| A. | 都能与Fe反应生成FeCl3 | B. | 与AgNO3溶液反应都生成白色沉淀 | ||
| C. | 均有毒 | D. | 都具有氧化性 |
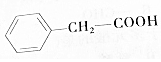 苯乙酸
苯乙酸 .
.
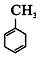 的官能团名称为碳碳双键.
的官能团名称为碳碳双键. 的系统命名为2-丙酮酸,则A的名称是3-丁酮酸.
的系统命名为2-丙酮酸,则A的名称是3-丁酮酸.
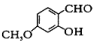 中能与稀NaOH溶液反应的官能团是羟基.检验该官能团的方法是取少量样品,加入氯化铁溶液,如果显紫色,则说明含有酚羟基.
中能与稀NaOH溶液反应的官能团是羟基.检验该官能团的方法是取少量样品,加入氯化铁溶液,如果显紫色,则说明含有酚羟基.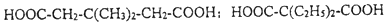 .
.
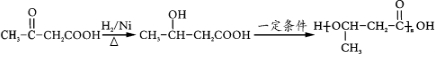 .(无机试剂任用)
.(无机试剂任用)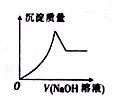 某水溶液X中只可能含有Al3+、CO32-、Cl-、SiO32-、SO42-、Fe2+中的若干种离子.某同学对该溶液进行了如下实验:
某水溶液X中只可能含有Al3+、CO32-、Cl-、SiO32-、SO42-、Fe2+中的若干种离子.某同学对该溶液进行了如下实验: