题目内容
有A、B、C、D四种金属.将A与B用导线连接起来,浸入电解质溶液中,B为正极.将A、D分别投入等浓度盐酸中,D比A反应剧烈.将铜浸入B的盐溶液里,无明显变化.如果把铜浸入C的盐溶液里,有金属C析出.据此判断它们的活动性由强到弱的顺序是( )
| A、D A B C |
| B、D C A B |
| C、B A D C |
| D、A B C D |
考点:原电池和电解池的工作原理,常见金属的活动性顺序及其应用
专题:电化学专题
分析:原电池中被腐蚀的金属是活动性强的金属;金属和相同的酸反应时,活动性强的金属反应剧烈;金属的置换反应中,较活泼金属能置换出较不活泼的金属.
解答:
解:两种活动性不同的金属和电解质溶液构成原电池,较活泼的金属作负极,负极上金属失电子发生氧化反应被腐蚀,较不活泼的金属作正极,将A与B用导线连接起来浸入电解质溶液中,B为正极,所以A的活动性大于B.
金属和相同的酸反应时,活动性强的金属反应剧烈,将A、D分别投入等浓度盐酸溶液中,D比A反应剧烈,所以D的活动性大于A;
金属的置换反应中,较活泼金属能置换出较不活泼的金属,将铜浸入B的盐溶液中,无明显变化,说明B的活动性大于铜.如果把铜浸入C的盐溶液中,有金属C析出,说明铜的活动性大于C,则活动性B>Cu>C;
所以金属的活动性顺序为:D>A>B>C,
故选A.
金属和相同的酸反应时,活动性强的金属反应剧烈,将A、D分别投入等浓度盐酸溶液中,D比A反应剧烈,所以D的活动性大于A;
金属的置换反应中,较活泼金属能置换出较不活泼的金属,将铜浸入B的盐溶液中,无明显变化,说明B的活动性大于铜.如果把铜浸入C的盐溶液中,有金属C析出,说明铜的活动性大于C,则活动性B>Cu>C;
所以金属的活动性顺序为:D>A>B>C,
故选A.
点评:本题考查了金属活动性强弱的判断,难度不大,能从原电池的负极、金属之间的置换反应、金属与酸或水反应的剧烈程度、金属氧化物的水化物的碱性强弱等方面来判断金属的活动性强弱.

练习册系列答案
相关题目
下列实验操作中存在有不合理操作的是( )
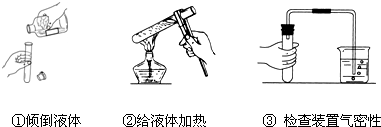

| A、①② | B、①③ | C、①②③ | D、②③ |
将一小块钠投入到NH4Cl溶液中,产生的气体是( )
| A、O2和H2 |
| B、只有H2 |
| C、只有NH3 |
| D、H2和NH3 |
下列物质的沸点排列顺序不正确的是( )
| A、H2O>H2Te>H2Se>H2S |
| B、He>Ne>Ar>Kr |
| C、I2>Br2>Cl2>F2 |
| D、GeH4>SiH4>CH4 |
将足量SO2通入下列各溶液中,所含离子还能大量共存的是( )
| A、K+、Ba2+、Cl-、NO3- |
| B、Mg2+、Ca2+、NH4+、Cl- |
| C、Na+、H+、S2O32-、SO42- |
| D、Na+、AlO2-、CH3COO-、ClO- |
下列反应的离子方程式书写正确的是( )
| A、NaHCO3的水解:HCO3-+H2O?H3O++CO32- | ||||
| B、硫酸亚铁溶液中加入过氧化氢溶液:2Fe2++H2O2+2H+=2Fe3++2H2O | ||||
| C、硫酸铜溶液中加入氢氧化钡溶液:Ba2++SO42-=BaSO4↓ | ||||
D、除去KNO3溶液中的Fe3+:Fe3++3H2O
|
下列化学反应的离子方程式正确的是( )
(1)向CH2ClCOOH中加入足量的氢氧化钠溶液并加热:CH2ClCOOH+OH-
CH2ClCOO-+H2O
(2)在稀氨水中通入过量CO2:NH3?H2O+CO2═NH4++HCO3-
(3)少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO
(4)氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O
(5)向小苏打溶液中加入过量的澄清石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O
(6)向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+
(7)向磷酸二氢铵溶液中加入足量的氢氧化钠溶液:NH3-+OH-═NH3?H2O
(8)用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑
(1)向CH2ClCOOH中加入足量的氢氧化钠溶液并加热:CH2ClCOOH+OH-
| △ |
(2)在稀氨水中通入过量CO2:NH3?H2O+CO2═NH4++HCO3-
(3)少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO
(4)氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O
(5)向小苏打溶液中加入过量的澄清石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O
(6)向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+
(7)向磷酸二氢铵溶液中加入足量的氢氧化钠溶液:NH3-+OH-═NH3?H2O
(8)用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑
| A、(2)(3)(5) |
| B、(3)(4)(6) |
| C、(1)(3)(5)(7)(8) |
| D、(2)(5)(6) |
下列十二种物质中:Fe、CaO、SO3、盐酸、硫酸、KOH溶液、NH4HCO3、CCl4、NH3?H2O、HF、BaSO4、熔融的KCl.其中属于强电解质、弱电解质、非电解质的物质种类依次为( )
| A、5、2、2 |
| B、7、3、2 |
| C、6、2、4 |
| D、5、3、4 |