题目内容
有机物
H3
H═
H-
≡CH中标有“?”的碳原子的杂化方式依次为( )
| C |
| ? |
| C |
| ? |
| C |
| ? |
| C |
| ? |
| A、sp、sp2、sp3 |
| B、sp3、sp2、sp |
| C、sp2、sp、sp3 |
| D、sp3、sp、sp2 |
考点:原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:根据价层电子对互斥理论判断C原子杂化方式,价层电子对个数=σ键个数+孤电子对个数,如果价层电子对个数是4,则C原子采用sp3杂化,如果价层电子对个数是3,则C原子采用sp2杂化,如果价层电子对个数是2,则C原子采用sp杂化,据此分析解答.
解答:
解:根据价层电子对互斥理论判断C原子杂化方式,价层电子对个数=σ键个数+孤电子对个数,如果价层电子对个数是4,则C原子采用sp3杂化,如果价层电子对个数是3,则C原子采用sp2杂化,如果价层电子对个数是2,则C原子采用sp杂化,
甲基上C原子含有4个σ键,则C原子采用sp3杂化,碳碳双键两端的C原子含有3个σ键,则C原子采用sp2杂化,碳碳三键两端的C原子含有2个σ键,则C原子采用sp杂化,
故选B.
甲基上C原子含有4个σ键,则C原子采用sp3杂化,碳碳双键两端的C原子含有3个σ键,则C原子采用sp2杂化,碳碳三键两端的C原子含有2个σ键,则C原子采用sp杂化,
故选B.
点评:本题考查原子杂化方式判断,明确价层电子对互斥理论是解本题关键,知道价层电子对个数的计算方法,为考试高频点,题目难度中等.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
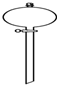
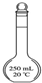
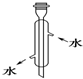
下列装置或操作能达到实验目的是( )
A、 除去乙醇中的乙酸 |
B、 形成原电池 |
C、 制取乙酸乙酯 |
D、 石油的分馏 |
研究表明,化学反应中的能量变化其本质是化学键的生成或断裂过程中分别会释放与吸收能量.如图表示反应2H2(g)+O2(g)═2H2O(g)的能量变化,下列有关说法中错误的是( )


| A、图中的①是指吸收能量,②是指放出能量 |
| B、图示说明反应2H2(g)+O2(g)═2H2O(g)是一个吸热反应 |
| C、图示说明化学键的形成与断裂是物质在化学反应中发生能量变化的主要原因 |
| D、③中a所指的数值为484 |
pH值测定是检验物质的常用方法,下列有关pH值测定的实验合理的是( )
| A、将失去标签的Na2CO3和NaHCO3固体样品配成等物质的量浓度溶液,分别测定pH值,以此鉴别这两种固体 |
| B、用pH试纸分别测定氯水和盐酸的pH值,比较两溶液的酸性强弱 |
| C、取同体积不同浓度的醋酸和盐酸加水稀释相同倍数,测定稀释前后pH值的变化,以此区别这两种酸 |
| D、测定硫酸型酸雨的pH值时,取样后应立即测定 |
自然科学史中很多发现和发明都是通过类比推理法提出来的.现有化合物A的结构简式
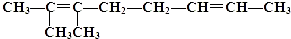 .它与过量的酸性高锰酸钾溶液作用得到下列三种化合物:
.它与过量的酸性高锰酸钾溶液作用得到下列三种化合物: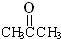 ,
,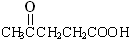 ,CH3COOH.若化合物B与A互为同分异构体,且A、B分别与酸性高锰酸钾溶液反应得到的产物相同,则化合物B的结构简式正确的是( )
,CH3COOH.若化合物B与A互为同分异构体,且A、B分别与酸性高锰酸钾溶液反应得到的产物相同,则化合物B的结构简式正确的是( )
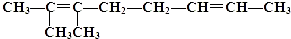 .它与过量的酸性高锰酸钾溶液作用得到下列三种化合物:
.它与过量的酸性高锰酸钾溶液作用得到下列三种化合物: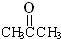 ,
,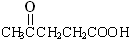 ,CH3COOH.若化合物B与A互为同分异构体,且A、B分别与酸性高锰酸钾溶液反应得到的产物相同,则化合物B的结构简式正确的是( )
,CH3COOH.若化合物B与A互为同分异构体,且A、B分别与酸性高锰酸钾溶液反应得到的产物相同,则化合物B的结构简式正确的是( )| A、CH3CH=C(CH3)-(CH2)2-C(CH3)=CHCH3 |
| B、(CH3)2C=CH-(CH2)2-C(CH3)=CHCH3 |
| C、(CH3)2C=C(CH3)-(CH2)2-CH=CHCH3 |
| D、( CH3)2C=CH-(CH2)2-CH=C(CH3)2 |