题目内容
8.下列说法不正确的是( )| A. | 用新制氢氧化铜悬浊液可以鉴别乙酸、葡萄糖和淀粉三种溶液 | |
| B. | 用重铬酸钾溶液检验司机是否酒驾所发生的反应属于乙醇的氧化反应 | |
| C. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 | |
| D. | 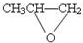 和CO2反应生成可降解聚合物 和CO2反应生成可降解聚合物 ,该反应不符合绿色化学原则 ,该反应不符合绿色化学原则 |
分析 A.乙酸具有酸性,葡萄糖含有醛基,能与新制备氢氧化铜悬浊液反应,淀粉为非还原性糖;
B.乙醇被重铬酸钾溶液氧化生成乙酸;
C.铜催化作用下乙醇被氧化;
D.该反应过程原子利用率达100%.
解答 解:A.新制Cu(OH)2与乙酸反应蓝色絮状沉淀渐渐消失,有蓝色溶液生成,与葡萄糖溶液混合加热生成砖红色沉淀、与淀粉溶液无明显现象,故A正确;
B.乙醇被重铬酸钾溶液氧化生成乙酸,所以该反应属于氧化反应,故B正确;
C.铜丝在酒精灯上加热后产生氧化铜,反应的方程式为2Cu+O2=2CuO,立即伸入无水乙醇中,发生的反应方程式为CuO+CH3CH2OH$\stackrel{△}{→}$Cu+CH3CHO+H2O,因此铜丝恢复成原来的红色,故C正确;
D.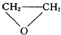 和CO2反应生成可降解聚合物[O-CHCH2-O-CO]n,该反应过程原子利用率达100%,所以该反应符合绿色化学的原则,故D错误.
和CO2反应生成可降解聚合物[O-CHCH2-O-CO]n,该反应过程原子利用率达100%,所以该反应符合绿色化学的原则,故D错误.
点评 本题考查有机物的结构和性质,为高频考点,涉及有机物鉴别、制备及性质等,把握官能团与性质的关系及制备原理为解答的关键,题目难度不大.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
19.有关下列电化学装置的说法中正确的是( )
| A. | 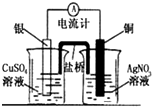 图是原电池装置,可以实现化学能转化为电能 | |
| B. | 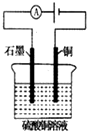 图电解一段时间后,加入适量CuO固体,可以使硫酸铜溶液恢复到原浓度 | |
| C. | 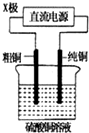 图中的X极若为负极,则该装置可实现粗铜的精炼 | |
| D. | 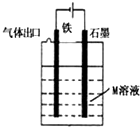 图中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀 |
16.下列有机物的一氯代物是四种的是( )
①异戊烷 ②甲苯 ③2-丁烯 ④对二甲苯.
①异戊烷 ②甲苯 ③2-丁烯 ④对二甲苯.
| A. | ①② | B. | ①③ | C. | ②④ | D. | ③④ |
3.化合物的 二氯代物的同分异构体数目为( )
二氯代物的同分异构体数目为( )
 二氯代物的同分异构体数目为( )
二氯代物的同分异构体数目为( )| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |
13.两种气态烃的混和物共0.1mol,完全燃烧后得到3.36L(标准状况下)CO2和3.6g水,下列说法正确的是( )
| A. | 可能有甲烷 | B. | 一定有乙烯 | C. | 可能有乙烷 | D. | 可能有乙烯 |
17.现有7种元素的性质、数据如表所列,它们属于第二或第三周期.
回答下列问题:
(1)③原子结构示意图是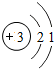 ,⑤的氢化物和⑦的氢化物形成化合物的电子式
,⑤的氢化物和⑦的氢化物形成化合物的电子式 .
.
(2)在最高价氧化物的水化物中,碱性最强的化合物的电子式是: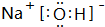 ; 属离子化合物(填“离子”或“共价”).
; 属离子化合物(填“离子”或“共价”).
(3)比较④和⑦的氢化物的稳定性(用化学式表示):NH3>PH3.
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:NH3+HNO3=NH4NO3.
编号 性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | |
| -2 | -3 | -1 | -3 |
(1)③原子结构示意图是
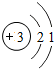 ,⑤的氢化物和⑦的氢化物形成化合物的电子式
,⑤的氢化物和⑦的氢化物形成化合物的电子式 .
.(2)在最高价氧化物的水化物中,碱性最强的化合物的电子式是:
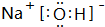 ; 属离子化合物(填“离子”或“共价”).
; 属离子化合物(填“离子”或“共价”).(3)比较④和⑦的氢化物的稳定性(用化学式表示):NH3>PH3.
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:NH3+HNO3=NH4NO3.
18.下面实验操作不能实现实验目的是( )
| 实验操作 | 目的 | |
| A | 取绿豆大的钠分别加入到水和乙醇中 | 证明乙醇羟基中氢原子不如水分 子中氢原子活泼 |
| B | 取绿豆大的钠与钾分别投入水中 | 证明钾的金属性强于钠 |
| C | 将石蜡油在催化作用下,加强热产生的气 体通入溴的四氯化碳溶液中 | 证明产物不都是烷烃 |
| D | 加热乙酸乙酯、乙醇和乙酸的混合物 | 除去乙酸乙酯中的乙醇和乙酸 |
| A. | A | B. | B | C. | C | D. | D |
 下列关于晶体的说法正确的组合是( )
下列关于晶体的说法正确的组合是( ) 一家人其乐融融地坐在大彩电前欣赏精彩的电视剧是一件很温馨的事情,带给我们幸福的大彩电离不开高分子物质,其中制造彩电荧光屏的高分子材料具有感光性,称为“光敏性高分子”,其结构简式如图所示.
一家人其乐融融地坐在大彩电前欣赏精彩的电视剧是一件很温馨的事情,带给我们幸福的大彩电离不开高分子物质,其中制造彩电荧光屏的高分子材料具有感光性,称为“光敏性高分子”,其结构简式如图所示.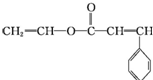 ,该单体可由
,该单体可由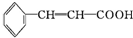 和CH2=CH-OH经酯化(或取代)反应(填反应类型)得到.
和CH2=CH-OH经酯化(或取代)反应(填反应类型)得到.