题目内容
13.两种气态烃的混和物共0.1mol,完全燃烧后得到3.36L(标准状况下)CO2和3.6g水,下列说法正确的是( )| A. | 可能有甲烷 | B. | 一定有乙烯 | C. | 可能有乙烷 | D. | 可能有乙烯 |
分析 n(CO2)=$\frac{3.36L}{22.4L/mol}$=0.15mol,n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,则混合的平均化学式为C1.5H4,因是混合物,则肯定含有C原子数小于1.5的烃,即一定含有甲烷,因甲烷中含有4个氢原子,则另一种烃也含有4个氢原子,以此解答该题.
解答 解:n(CO2)=$\frac{3.36L}{22.4L/mol}$=0.15mol,n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,则混合的平均化学式为C1.5H4,
因是混合物,则肯定含有C原子数小于1.5的烃,所以一定含有甲烷,因甲烷中含有4个氢原子,则另一种烃也含有4个氢原子,可能为乙烯、丙炔等,一定不含乙烷,
选项中只有D符合,
故选D.
点评 本题考查了有机物分子式确定的计算,题目难度不大,明确平均分子式的含义及应用方法为解答关键,注意掌握守恒思想在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.从柑橘中可提炼得到1,8-萜二烯: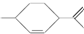 ,下列有关该有机物的说法中不正确的是( )
,下列有关该有机物的说法中不正确的是( )
 ,下列有关该有机物的说法中不正确的是( )
,下列有关该有机物的说法中不正确的是( )| A. | 分子式为C10H18 | |
| B. | 常温下呈液态,难溶于水 | |
| C. | 1 mol该有机物最多能和2mol H2发生加成反应 | |
| D. | 该有机物能与溴水发生取代反应 |
1.B3N3H6的结构和性质与苯相似,因而称为无机苯.下列关于无机苯的叙述不正确的是( )
| A. | 无机苯中各原子在同一平面上 | |
| B. | 无机苯为实际上是有机物 | |
| C. | 在一定条件下,无机苯可发生取代反应和加成反应 | |
| D. | 无机苯不能使酸性KMnO4溶液褪色 |
8.下列说法不正确的是( )
| A. | 用新制氢氧化铜悬浊液可以鉴别乙酸、葡萄糖和淀粉三种溶液 | |
| B. | 用重铬酸钾溶液检验司机是否酒驾所发生的反应属于乙醇的氧化反应 | |
| C. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 | |
| D. | 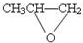 和CO2反应生成可降解聚合物 和CO2反应生成可降解聚合物 ,该反应不符合绿色化学原则 ,该反应不符合绿色化学原则 |
18.已知含有羧基的物质具有和乙酸相似的性质.巴豆酸是一种对胃肠道有强烈刺激性、对呼吸中枢和心脏有麻痹作用的有机酸,其结构简式为CH3-CH═CH-COOH,一定条件下下列物质中能与巴豆酸反应的是( )
①氯化氢 ②溴水 ③纯碱溶液 ④乙醇 ⑤酸化的KMnO4溶液.
①氯化氢 ②溴水 ③纯碱溶液 ④乙醇 ⑤酸化的KMnO4溶液.
| A. | 只有②④⑤ | B. | 只有①③④ | C. | 只有①②③④ | D. | ①②③④⑤ |
5.设NA代表阿伏加德罗常数(NA)的数值,下列说法正确的是( )
| A. | 标准状况下,2.24L戊烷所含分子数为0.1 NA | |
| B. | 乙烯和环丙烷(C3H6)组成的28g混合气体中含有4NA个氢原子 | |
| C. | 17.6g丙烷中所含的极性共价键为4NA个 | |
| D. | 常温常压下,22.4L乙烯中C-H键数为NA |
2.化学与科学、技术、社会、环境密切相关.下列有关说法中,正确的是( )
| A. | 钢、青铜、硬铝和金刚石都是合金材料 | |
| B. | 铝合金的熔点和硬度均高于纯铝 | |
| C. | 铝合金的大量使用是因为人们能用焦炭等还原剂从氧化铝中获得铝 | |
| D. | 不锈钢和目前流通的硬币都是合金 |
3.下列说法中正确的是( )
| A. | 0.1 mol•L-1盐酸和0.1 mol•L-1硫酸与2 mol•L-1 NaOH溶液反应速率相同 | |
| B. | 大理石块和大理石粉与0.1 mol•L-1盐酸反应的速率相同 | |
| C. | 等量的Mg粉、Al粉和0.1 mol•L-1盐酸反应速率相同 | |
| D. | 0.1 mol•L-1盐酸和0.1 mol•L-1硝酸与相同形状和大小的大理石反应的速率相同 |