题目内容
已知金刚石晶体中C-C键键能为348kJ/mol,氧气中1mol O=O键完全断裂时吸收热量496kJ,二氧化碳气体中1mol C=O键键能为799kJ/mol,则12g金刚石晶体完全燃烧生成二氧化碳气体的反应热为 .
考点:有关反应热的计算
专题:化学反应中的能量变化
分析:根据反应热等于反应物的总键能-生成物的总键能,注意金刚石键能的计算.
解答:
解:根据C+O2
CO2可知12g金刚石晶体完全燃烧需要1mol氧气生成1mol二氧化碳气体,
12g金刚石晶体中键能为348kJ/mol×2=696kJ/mol,
1mol氧气中键能为496kJ/mol
1mol二氧化碳气体中键能为799kJ/mol×2=1598kJ/mol,
所以反应热为696kJ/mol+496kJ/mol-1598kJ/mol=-406kJ/mol,
故答案为:-406kJ/mol.
| ||
12g金刚石晶体中键能为348kJ/mol×2=696kJ/mol,
1mol氧气中键能为496kJ/mol
1mol二氧化碳气体中键能为799kJ/mol×2=1598kJ/mol,
所以反应热为696kJ/mol+496kJ/mol-1598kJ/mol=-406kJ/mol,
故答案为:-406kJ/mol.
点评:本题主要考查了反应热的计算,难度不大,根据反应热等于反应物的总键能-生成物的总键能即可完成.

练习册系列答案
相关题目
已知室温时,0.1mol/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是( )
| A、升高温度,溶液的pH增大 |
| B、室温时,此酸的电离平衡常数约为1×10-7 |
| C、该溶液的pH=4 |
| D、升高温度,电离平衡常数增大 |
下列说法正确的是( )
| A、SiH4比CH4稳定 |
| B、P和As属于第ⅤA族元素,H3PO4酸性比H3AsO4的强 |
| C、Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强 |
| D、O2-半径比F-的小 |

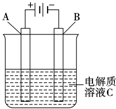 肼(N2H4)又称联氨,是一种可燃性液体,与氧气或氮氧化物反应均生成氮气和水,可作火箭燃料.
肼(N2H4)又称联氨,是一种可燃性液体,与氧气或氮氧化物反应均生成氮气和水,可作火箭燃料.
 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.