题目内容
12.下列关于化学反应速率的说法正确的是( )| A. | 化学反应速率是对可逆反应而言的,非可逆反应不谈化学反应速率 | |
| B. | 对于可逆反应来说,升高温度,正反应速率与逆反应速率均会增大 | |
| C. | 化学反应速率为0.8 mol•L-1•s-1的含义是为1s时,物质的量浓度是0.8 mol•L-1 | |
| D. | 0.1 mol•L-1盐酸和0.1 mol•L-1醋酸与形状和大小相同的大理石反应的速率相同 |
分析 A.化学反应速率是对于所有的化学反应而言的;
B.升高温度,增大活化分子百分数;
C.化学反应速率为单位时间内浓度的变化;
D.醋酸为弱酸,氢离子浓度比盐酸小.
解答 解:A.化学反应速率是指单位时间内物质的量浓度的变化,对于所有的化学反应而言的,故A错误;
B.升高温度,增大活化分子百分数,正逆反应速率都增大,故B正确;
C.化学反应速率为单位时间内浓度的变化,化学反应速率为0.8 mol•L-1•s-1的含义是1s内浓度变化为0.8 mol•L-1,故C错误;
D.醋酸为弱酸,氢离子浓度比盐酸小,盐酸反应速率较大,故D错误.
故选B.
点评 本题考查化学反应素的影响因素,为高频考点,侧重于学生的分析能力和基本概念、理论知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
10.氢气可以在氧气中燃烧,已知1mol H2的键能为Q1KJ•mol-1,1mol O2的键能为Q2KJ•mol-1,1mol H2O的键能为Q3KJ•mol-1.下列关系式中,正确的是( )
| A. | 2Q1+Q2>Q3 | B. | Q1+Q2>2Q3 | C. | 2Q1+Q2<4Q3 | D. | 2Q1+Q2<2Q3 |
20.某周期第ⅡA族元素的原子序数为x,则同周期第ⅣA族元素的原子序数是( )
| A. | 只有x+2 | B. | 可能是x+2 或x+10或x+24 | ||
| C. | 可能是x+24 | D. | 可能是x+2或x+12或x+26 |
7.下列除杂方法中正确的一组是( )
| A. | 溴苯中混有溴,加入碘化钾溶液后用汽油萃取 | |
| B. | 乙酸乙酯中混有乙酸,加入 NaO H 溶液加热后用分液漏斗分液 | |
| C. | 乙烷中混有乙烯,通过盛有酸性 KMnO4 溶液的洗气瓶洗气 | |
| D. | 乙醇中混有水,加入生石灰,再加热蒸馏 |
17.已知反应:2H2O2═2H2O+O2↑,下列条件下,反应速率最大的是( )
| A. | 10℃,5 mL 3% H2O2溶液 | |
| B. | 10℃,5 mL 5% H2O2溶液 | |
| C. | 30℃,5 mL 5% H2O2溶液 | |
| D. | 30℃,5 mL 5% H2O2溶液且加入少量MnO2 |
4.下列化学用语表示正确的是( )
| A. | 苯的结构简式:C6H6 | B. | 二氧化碳的电子式: | ||
| C. | KNO3电离方程式:KNO3=K++NO3- | D. | Cl-的结构示意图: |
1.设NA为阿伏加德罗常数.下列说法正确的是( )
| A. | 常温常压下,20 g D2O分子中所含中子数为10 NA | |
| B. | 0.1 mol FeCl3水解生成的Fe(OH)3胶粒数为0.1 NA | |
| C. | 将lmol Cl2通入水中,HC1O、Cl-、C1O-粒子数之和为2 NA | |
| D. | 常温常压下,11.2 L CO2 与足量Na2O2反应转移的电子数为0.5 NA |
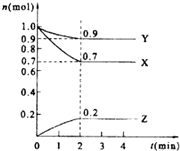 某温度时.在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示.
某温度时.在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示.