题目内容
11.在水溶液中YOn-3与S2-发生反应的离子方程式如下:YOn-3+3S2-+6H+=Y-+3S↓+3H2O,则YOn-3中Y元素的化合价和Y元素原子的最外层电子数分别是( )| A. | +5、4 | B. | +5、7 | C. | +5、5 | D. | +7、7 |
分析 利用离子方程式电荷守恒可知n=1,再利用YO3n-中各元素的化合价代数和等于-1计算YO3n-中Y的化合价;由于Y元素形成Y-离子,可知Y元素的最低化合价为-1价,最低负化合价=最外层电子数-8,据此计算Y原子最外层电子数.
解答 解:根据电荷守恒可知:-n+3×(-2)+6=-1,解得n=1.
令YO3n-中Y元素的化合价为x,则:x+3×(-2)=-1,解得x=+5.
由于Y元素形成Y-离子,可知Y元素的最低化合价为-1价,由于最低负化合价=最外层电子数-8,
所以Y原子最外层电子数=8-1=7.
故选B.
点评 本题考查离子方程式、氧化还原反应等,难度不大,可以根据电子转移守恒计算YO3n-中Y元素化合价,注意守恒思想的运用.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
1.化学与生活、社会发展息息相关,下列有关说法正确的是( )
| A. | 侯氏制碱法的工艺过程中主要应用了物质熔沸点的差异 | |
| B. | “熬胆矾铁釜,久之亦化为铜”,该过程发生了分解反应 | |
| C. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于物理变化 | |
| D. | 钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 |
6.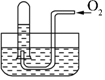 如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管.当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体( )
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管.当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体( )
 如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管.当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体( )
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管.当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体( )| A. | 可能是N2与NO2的混合气体 | B. | 可能是O2与NO2的混合气体 | ||
| C. | 一定是NO与NO2的混合气体 | D. | 只可能是NO2一种气体 |
16.如下六个图中,横坐标为某溶液中加入某物质的物质的量,纵坐标为生成沉淀的物质的量,将图中的字母代号填入下表.


| 溶液 | 加入的物质 | 字母代号 |
| ①饱和石灰水 | 通过量CO2 | B |
| ②AlCl3溶液 | 通过量NH3 | C |
| ③MgCl2、AlCl3混合溶液 | 逐滴加NaOH溶液至过量 | A |
| ④AlCl3溶液 | 逐滴加NaOH溶液至过量 | E |
| ⑤含少量HCl的AlCl3溶液 | 逐滴加NaOH溶液至过量 | F |
1.下列说法中,正确的是( )
| A. | 分子间作用力越大,分子越稳定 | |
| B. | 气态氢化物共价键越强,热稳定性越高 | |
| C. | 冰融化时水分子中共价键发生断裂 | |
| D. | 氢键是化学键的一种类型 |
2.下列装置或操作(有的夹持装置已省略)正确且能达到目的是( )
| A. | 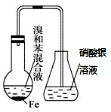 验证苯和液溴在催化剂作用下发生取代反应 | |
| B. | 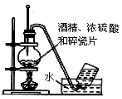 实验室制备并收集乙烯 | |
| C. | 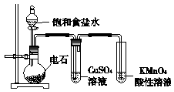 制备乙炔并检验其性质 | |
| D. | 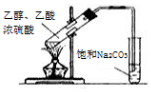 乙醇与乙酸反应制备乙酸乙酯 |
 ;
; ;
;