题目内容
在一个不传热的固定容积的密闭容器中发生可逆反应:mA(g)+nB(g)?pC(g)+qD(g),当m、n、p、q为任意整数(不为零)时,不能说明达到平衡状态的标志是( )
| A、D的质量不再改变 |
| B、各组分的浓度不再改变 |
| C、反应速率υA:υB:υC:υD=m:n:p:q |
| D、单位时间内m mol A断键发生反应,同时p mol C也断键发生反应 |
考点:化学平衡状态的判断
专题:
分析:根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A、D的质量不再改变,说明正逆反应速率相等,达平衡状态,故A正确;
B、各组分的浓度不再改变,说明正逆反应速率相等,达平衡状态,故B正确;
C、反应速率υA:υB:υC:υD=m:n:p:q,而不是不变,故C错误;
D、单位时间内m mol A断键等效于p mol C形成,同时p mol C也断键发生反应,正逆反应速率相等,达平衡状态,故D正确;
故选C.
B、各组分的浓度不再改变,说明正逆反应速率相等,达平衡状态,故B正确;
C、反应速率υA:υB:υC:υD=m:n:p:q,而不是不变,故C错误;
D、单位时间内m mol A断键等效于p mol C形成,同时p mol C也断键发生反应,正逆反应速率相等,达平衡状态,故D正确;
故选C.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
如图是常见四种有机物的比例模型示意图.下列说法正确的是( )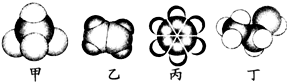

| A、甲能使酸性高锰酸钾溶液褪色 |
| B、乙可与溴水发生取代反应使溴水褪色 |
| C、丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特的共价键 |
| D、丁与乙酸都能发生发生中和反应 |
化学在生产和日常生活中有着重要的应用.下列说法中不正确的是( )
| A、明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| B、日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 |
| C、用Al(OH)3制胃酸过多 |
| D、电解AlCl3饱和溶液,可制得金属铝 |
已知Cu+在酸性条件下能发生下列反应:Cu+→Cu+Cu2+ (未配平).NH4CuSO3与足量的10mol/LH2SO4溶液混合微热,产生下列现象据此判断下列说法一定合理的是( )
①有红色金属生成 ②有刺激性气味气体产生 ③溶液呈蓝色.
①有红色金属生成 ②有刺激性气味气体产生 ③溶液呈蓝色.
| A、反应中硫酸作氧化剂 |
| B、该反应显示硫酸具有酸性 |
| C、刺激性气味的气体是氨气 |
| D、NH4CuSO3中铜元素全部被氧化 |
下列实验操作或对实验事实的叙述正确的是( )
| A、将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 |
| B、用碱式滴定管量取20.00mL0.1mol/LKMnO4溶液 |
| C、向沸腾的NaOH溶液中滴加FeCl3溶液,制备Fe(OH)3胶体 |
| D、配制FeSO4溶液时,需加入少量铁粉和稀硫酸 |
下列化学反应中反应类型与其它反应不同的是(反应条件略)( )
A、HOCH2CH2CH2CH2COOH?H2O+ |
| B、CH2BrCH2Br+2NaOH→CH≡CH↑+2NaBr+2H2O |
| C、CH3CHOHCH3→CH2=CHCH3↑+H2O |
| D、CH3CH2Cl→CH2=CH2↑+H2O |