��Ŀ����
16��AԪ�ص�һ�ֵ�����һ����Ҫ�İ뵼����ϣ���AԪ�ص�һ�ֻ�����C��������������ܵ��ִ�ͨѶ����--���ά��C���ռӦ���ɺ�AԪ�صĻ�����D����1��д��C���ᷢ����Ӧ�Ļ�ѧ����ʽ��SiO2+4HF�TSiF4��+2H2O��
��2����C�봿���ϸ�������ʱҲ������ѧ��Ӧ����D��ͬʱ������B�����������E����ȫ����E��ȫ����D��������ˮ�л�Ϻ��ַ�����ѧ��Ӧ���ɺ�A�Ļ�����F��
�ٷֱ�д������D��F�Ļ�ѧ����ʽ��SiO2+Na2CO3$\frac{\underline{\;����\;}}{\;}$Na2SiO3+CO2��Na2SiO3+CO2+H2O=Na2CO3+H2SiO3����
��Ҫ��NaOH�����ۻ������������п�ѡ�õ���D��
A����ͨ�������� B��ʯӢ�������� C������������ D��������
��3��100g C��ʯ��ʯ�Ļ�����ַ�Ӧ�����ɵ������ڱ���µ����Ϊ11.2L��100g�������ʯ��ʯ������������50%��
���� ��AԪ�ص�һ�ֵ�����һ����Ҫ�İ뵼����ϣ���AΪSi����AԪ�ص�һ�ֻ�����C��������������ܵ��ִ�ͨѶ����--���ά����CΪSiO2��C���ռӦ���ɺ�AԪ�صĻ�����DΪNa2SiO3���ɴ˷������
��� �⣺��AԪ�ص�һ�ֵ�����һ����Ҫ�İ뵼����ϣ���AΪSi����AԪ�ص�һ�ֻ�����C��������������ܵ��ִ�ͨѶ����--���ά����CΪSiO2��C���ռӦ���ɺ�AԪ�صĻ�����DΪNa2SiO3��
��1����������������ᷴӦ�����ķ�������ˮ����Ӧ����ʽΪ��SiO2+4HF�TSiF4��+2H2O��
�ʴ�Ϊ��SiO2+4HF�TSiF4��+2H2O��
��2���ٽ�SiO2�봿���ϸ�������ʱ��Ӧ����Na2SiO3��ͬʱ������B�����������E����EΪCO2��BΪC����ȫ����CO2��ȫ����Na2SiO3��������ˮ�л�Ϻ������˺�A�Ļ�����FΪH2SiO3����Ӧ����ʽΪ��SiO2+Na2CO3$\frac{\underline{\;����\;}}{\;}$Na2SiO3+CO2����Na2SiO3+CO2+H2O=Na2CO3+H2SiO3����
�ʴ�Ϊ��SiO2+Na2CO3$\frac{\underline{\;����\;}}{\;}$Na2SiO3+CO2����Na2SiO3+CO2+H2O=Na2CO3+H2SiO3����
����ͨ����������ʯӢ�����������������еĶ��������Լ����������������¶������������Ʒ�Ӧ����ѡD��
�ʴ�Ϊ��D��
��3������Ҫ����Na2CO3��SiO2�Ļ�ѧ��Ӧȷ��CaCO3��SiO2�Ļ�ѧ��Ӧ��Ȼ��Ҫ�ҳ�CaCO3+SiO2$\frac{\underline{\;����\;}}{\;}$CaSiO3+CO2����CaCO3$\frac{\underline{\;����\;}}{\;}$CaO+CO2��������ѧ��Ӧ��n��CaCO3����n��CO2���Ĺ�ϵ��n��CaCO3��=n��CO2����
���ɱ�״����CO2����11.2L�������ʵ���=$\frac{11.2L}{22.4L/mol}$=0.5mol��
m��CaCO3��=0.5mol��100g/mol=50g
��Ʒ��̼��Ƶ�����������$\frac{50g}{100g}$��100%=50%
�ʴ�Ϊ��50%��
���� ���⿼�������ƶϡ�Ԫ�ػ��������ʣ����ڿ�������������ۺ�Ӧ��֪ʶ���������ѶȲ���ע��Ի���֪ʶ�����գ�

| A�� | ͬ���ڽ���Ԫ�صĻ��ϼ�Խ�ߣ���ԭ��ʧ��������Խǿ | |
| B�� | ͬ����Ԫ�صļ������ӻ�ԭ��Խǿ�����⻯��Խ�ȶ� | |
| C�� | �ڶ�����Ԫ�ش����ң�������۴�+1������+7 | |
| D�� | IA�����A��Ԫ�ؼ����γ����ӻ�����ۻ����� |
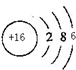
 ������Ԫ��X��Y��Z��W�����ڱ��е�λ����ͼ��ʾ������W�����������γ��������Ҫ����֮һ��
������Ԫ��X��Y��Z��W�����ڱ��е�λ����ͼ��ʾ������W�����������γ��������Ҫ����֮һ��| X | |||
| Z | W | Y |
 ��
����2����֪��
��X��s��+O2��g��=XO2��g����H=-393.5kJ•mol-1
��H2��g��+$\frac{1}{2}$O2��g��=H2O��g����H=-242.0kJ•mol-1
��XH4��g��+2O2��g��=XO2��g��+2H2O��g����H=-802.0kJ•mol-1
��XH4����ֽ��������X������Ȼ�ѧ����ʽΪCH4��g��=2H2��g��+C��s����H=+75.5kJ/mol��
��3��ZO���ɵ���X��ZO2��Ӧ��ȡ����Z���м��������м����ȶ�������������ʱ��ZO��NaOH��Һ��Ӧ�����ﺬ��һ�ֹ��嵥�ʺ�һ�����Σ��Ļ�ѧ����ʽΪ2SiO+2NaOH=Si+Na2SiO3+H2O��
��4��Ԫ��Y��Ca�κ�H2Ϊԭ�ϣ���Ӧ����ֻ�м��������Ҿ�Ϊ������о����֣������������иơ�Ԫ��Y�����������ֱ�Ϊ52.29%��46.41%���������ҵ�ˮ��Һ�����ԣ����ҵĻ�ѧʽΪHCl������ˮ��Ӧ�ɵ�H2���仯ѧ����ʽ�ǣ�2CaHCl+2H2O=CaCl2+Ca��OH��2+2H2����
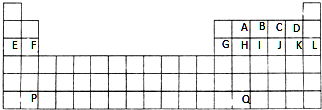
��5����W����̬�⻯��ͨ��һ������NaOH��Һ�У���������Һ����μ���ϡ����������������������HCl�����ʵ����Ĺ�ϵ��ͼ��ʾ������������ܽ��HCl�Ļӷ�����
��O����Һ���������ʵĻ�ѧʽΪNaOH��Na2S��
��a����Һ�У�c��Na+����c��Cl-��=5��3��
| A�� | NH4+��NO3-��K+��SO42- | B�� | CO32-��NO3-��HCO3-��Na+ | ||
| C�� | Na+��ClO-��AlO2-��NO3- | D�� | Cu2+��K+��Na+��SO42- |
 ��ͼΪij�¶��£�CuS��s����ZnS��s����FeS��s���ֱ�����Һ�дﵽ�����ܽ�ƽ�����Һ��S2-Ũ�ȣ�����������Ũ�ȱ仯�����������������ֳ����Ļ�����м����ᣬ�����ܽ����FeS��
��ͼΪij�¶��£�CuS��s����ZnS��s����FeS��s���ֱ�����Һ�дﵽ�����ܽ�ƽ�����Һ��S2-Ũ�ȣ�����������Ũ�ȱ仯�����������������ֳ����Ļ�����м����ᣬ�����ܽ����FeS�� ��1��������β����ȼ�ղ��������������������������CH4����ԭNOx���������������Ⱦ��
��1��������β����ȼ�ղ��������������������������CH4����ԭNOx���������������Ⱦ��

 ��
��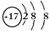 ��
��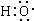
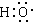 ���Ԫ����ͬ�����еĵ�����Ҳ��ͬ
���Ԫ����ͬ�����еĵ�����Ҳ��ͬ

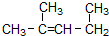 ����Ϊ1��3-����-2-��ϩ
����Ϊ1��3-����-2-��ϩ