题目内容
5.下列有关实验事实的解释正确的是( )| A. | 高锰酸钾溶液中通入SO2后,颜色褪去,SO2表现了漂白性 | |
| B. | 铁粉投入同浓度的Cu(NO3)2和AgNO3混合液先析出Ag,说明Ag+氧化性比Cu2+强 | |
| C. | 常温下,将铝片放入浓硫酸中无明显现象,说明铝和冷的浓硫酸完全不反应 | |
| D. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有吸水性 |
分析 A.紫红色是高锰酸根离子的颜色,通入二氧化硫气体溶液褪色是二氧化硫把高锰酸根还原为无色的锰离子;
B.氧化性越强,优先被铁粉还原;
C.铝片在常温下与浓硫酸发生了钝化现象,不是不反应;
D.该变化浓硫酸表现了脱水性,不是吸水性.
解答 解:A.二氧化硫具有还原性,SO2使酸性高锰酸钾溶液褪色是因为二者发生了氧化还原反应,而不是二氧化硫的漂白性,故A错误;
B.铁粉投入同浓度的Cu(NO3)2和AgNO3混合液,由于Ag+氧化性比Cu2+强,所以先析出Ag,故B正确;
C.由于浓硫酸与铝发生钝化现象,所以阻止了反应的继续进行,不是不反应,故C错误;
D.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性,不是吸水性,故D错误;
故选B.
点评 本题考查了化学实验方案的评价,题目难度不大,涉及二氧化硫漂白性、浓硫酸的性质、钝化现象及氧化还原反应等知识,明确常见元素及其化合物性质为解答关键,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
12.下列说法中正确的是( )
| A. | 植物油和裂化汽油都能使溴水褪色 | |
| B. | 葡萄糖、蔗糖都能与新制的Cu(OH)2悬浊液发生氧化反应 | |
| C. | 淀粉、油脂、氨基酸都能水解,但水解产物不同 | |
| D. | 天然植物油常温下一般呈液态,难溶于水,有恒定的熔沸点 |
13. 将Na2O2加入含有Al3+、Fe2+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示.下列说法不正确的是( )
将Na2O2加入含有Al3+、Fe2+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示.下列说法不正确的是( )
 将Na2O2加入含有Al3+、Fe2+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示.下列说法不正确的是( )
将Na2O2加入含有Al3+、Fe2+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示.下列说法不正确的是( )| A. | a=1.75 | |
| B. | b=0.5 | |
| C. | 原溶液中Al3+与Fe2+的物质的量之比为1:2 | |
| D. | 最后得到的沉淀为Fe(OH)3 |
13.下列有关sp杂化轨道的叙述正确的是( )
| A. | 是由一个1s轨道和一个2p轨道线性组合而成 | |
| B. | 等性sp杂化轨道中所含s、p的成分一样 | |
| C. | 等性sp杂化轨道有两个,一个能量升高,另一个能量降低,但总能量保持不变 | |
| D. | sp杂化轨道可与其他原子轨道形成σ键和π键 |
20.下列物质属于电解质的是( )
| A. | Cl2 | B. | KNO3 | C. | SO2 | D. | Al |
10.丙烯醛(结构简式为CH2=CH-CHO)能发生的化学反应有( )
①加成 ②消除(消去) ③取代 ④氧化 ⑤还原 ⑥加聚 ⑦缩聚.
①加成 ②消除(消去) ③取代 ④氧化 ⑤还原 ⑥加聚 ⑦缩聚.
| A. | ①③⑤⑦ | B. | ②④⑥ | C. | ①④⑤⑥ | D. | ③④⑤⑥ |
17.高炉炼铁中生成铁的反应一定是( )
| A. | 氧化还原反应 | B. | 置换反应 | C. | 复分解反应 | D. | 分解反应 |
14.下列物质的性质可以用“键能”来解释的是( )
| A. | SiO2熔点高 | B. | 氩气性质稳定 | C. | 碘易升华 | D. | NH3极易溶于水 |
15.下列化学用语所表示的微粒,对水的电离平衡没有影响的是( )
| A. | 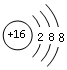 | B. | 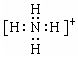 | C. | 1s22s22p63s1 | D. | 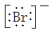 |