题目内容
若N表示阿伏加德罗常数的数值,在3(NH4)2SO4
N2↑+4NH3↑+3S02↑++H2O的反应中,当有N个电子转移时,以下说法中错误的是( )
| ||
A、有
| ||
B、有
| ||
C、有
| ||
D、有
|
考点:氧化还原反应
专题:
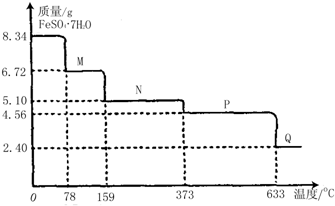
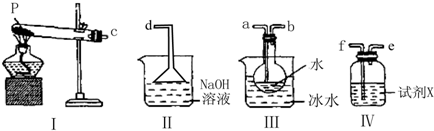
分析:(NH4)2SO4在强热分解的产物是SO2、N2、NH3和H2O,则N元素的化合价由-3价升高为0,S元素的化合价由+6价降低为+4,结合化合价的变化来解答.
解答:
解:A.反应中S元素化合价由+6价降低到+4价,被还原,则当有1mol电子转移时,有
molS02生成,所以当有N个电子转移时
N个S02生成,故A错误;
B.反应中S元素化合价由+6价降低到+4价,被还原,则当有1mol电子转移时,有
molS被还原,即当有N个电子转移时,有
个硫原子被还原,故B正确;
C.反应中S元素化合价由+6价降低到+4价,当1mol(NH4)2SO4分解时,转移2mol电子,则当有N个电子转移时,有
个硫酸铵分解,故C错误;
D.反应中N元素的化合价由-3价升高为0,当有N个电子转移时,有
个氮原子被氧化,故D正确.
故选AC.
| 1 |
| 2 |
| 1 |
| 2 |
B.反应中S元素化合价由+6价降低到+4价,被还原,则当有1mol电子转移时,有
| 1 |
| 2 |
| N |
| 2 |
C.反应中S元素化合价由+6价降低到+4价,当1mol(NH4)2SO4分解时,转移2mol电子,则当有N个电子转移时,有
| N |
| 2 |
D.反应中N元素的化合价由-3价升高为0,当有N个电子转移时,有
| N |
| 3 |
故选AC.
点评:本题考查氧化还原反应,为高考常见题型,把握反应中元素的化合价变化为解答的关键,由元素的化合价变化及电子守恒的角度解答该题,题目难度中等.

练习册系列答案
相关题目
在①甲烷、②乙烯、③苯、④乙醇四种分子中,分子内所有原子均在同一平面的是( )
| A、①② | B、②③ | C、③④ | D、②④ |
下列关于二氧化硅的说法中,正确的是( )
| A、因高温时SiO2与Na2CO3反应放出CO2,所以硅酸的酸性比碳酸强 |
| B、二氧化硅分子由一个硅原子和两个氧原子组成 |
| C、不能用二氧化硅跟水直接反应制取硅酸 |
| D、二氧化硅既能与氢氟酸反应,又能与烧碱反应,所以它是两性氧化物 |
将5.85g NaCl固体和19g MgCl2固体溶于水中得到100mL溶液,此溶液中Cl-的物质的量浓度为( )
| A、2mol/L |
| B、3mol/L |
| C、4mol/L |
| D、5mol/L |
判断下列概念及说法正确的是( )
| A、氧化还原反应:元素化合价是否变化 |
| B、纯净物与混合物:是否仅含有同种元素 |
| C、电解质与非电解质:溶液的导电能力大小 |
| D、溶液与胶体:本质不同的原因是能否发生丁达尔现象 |
在同温、同压条件下,两种物质的量相同的单质气体之间的关系( )
| A、体积都是22.4 L |
| B、具有相同的原子数目 |
| C、具有相同的体积 |
| D、都是双原子分子 |