题目内容
2.下列关于元素周期表和元素周期律的说法错误的是( )| A. | 因为K比Na容易失去电子,所以K比Na的还原性强 | |
| B. | 第二周期元素从Li到F,非金属性逐渐增强 | |
| C. | 在金属和非金属的分界线处,可以找到用于作催化剂的元素 | |
| D. | O与S为同主族元素,且O比S的非金属性强 |
分析 同周期元素的原子从左到右,元素非金属性逐渐增强;同主族元素的原子从上到下,元素非金属性逐渐减弱,电子层逐渐增多,失电子能力逐渐减弱,在金属元素与非金属元素的分界线附近的元素,通常既具有金属性又具有非金属性,可以找到半导体材料.
解答 解:A、Na与K比较,K更易失电子,还原性更强,故A正确;
B、根据元素周期律:同周期元素的原子从左到右,元素非金属性逐渐增强可推知第二周期元素从Li到F非金属性逐渐增强,故B正确;
C、在金属元素与非金属元素的分界线附近的元素,通常既具有金属性又具有非金属性,可以找到半导体材料,故C错误;
D、同主族元素的原子从上到下,元素非金属性逐渐减弱,O与S同主族,O的非金属性强,故D正确.
故选C.
点评 本题主要考查元素周期表的结构和应用,题目难度不大,本题根据元素周期表中的元素分布及元素常见的性质来解题,难度不大.

练习册系列答案
相关题目
12.下列与有机物结构、性质相关的叙述错误的是( )
| A. | 乙酸分子中含有羧基,可与NaHCO3溶液反应生成CO2 | |
| B. | 用福尔马林保鲜鱼肉等食品对人体有害 | |
| C. | 甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型不同 | |
| D. | 苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键 |
13.下列各组物质中,化学键的类型相同的是( )
| A. | CaCl2和Na2S | B. | Na2O和Na2O2 | C. | N2和Ne | D. | HCl和NaOH |
10.坚决反对运动员服用兴奋剂,是“人文奥运”的一个基本原则.某一种兴奋剂的结构简式为有关该有机物的说法不正确的是( )


| A. | 它可使酸性高锰酸钾溶液褪色,也能使溴水褪色 | |
| B. | 它属于芳香烃 | |
| C. | 它与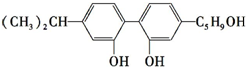 不是同分异构体 不是同分异构体 | |
| D. | 它既可发生加成反应,又可发生取代反应 |
17.下列化合物中阳离子和阴离子电子层结构相同的是( )
| A. | NaCl | B. | MgF2 | C. | CaF2 | D. | K2O |
11.下列操作会导致实验结果偏高的是( )
| A. | 中和热测定实验中,用铜制环形搅拌器代替环形玻璃搅拌棒,所测中和热的数值 | |
| B. | 中和滴定测定盐酸浓度,量取20.00mL盐酸时未用待测液润洗酸式滴定管 | |
| C. | 用托盘天平称量10.5g某物质,砝码和药品的位置放反,所称药品的质量 | |
| D. | 配制一定物质的量浓度溶液时,用量筒量取浓溶液体积仰视读数,所配溶液的浓度 |
8.由于碳碳双键不能自由旋转,因此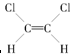 和
和 是两种不同的化合物,互为顺反异构体,则二溴丙烯的同分异构体(不含环状结构)有( )
是两种不同的化合物,互为顺反异构体,则二溴丙烯的同分异构体(不含环状结构)有( )
 和
和 是两种不同的化合物,互为顺反异构体,则二溴丙烯的同分异构体(不含环状结构)有( )
是两种不同的化合物,互为顺反异构体,则二溴丙烯的同分异构体(不含环状结构)有( )| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
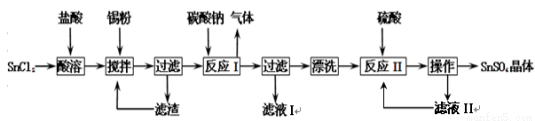
 ,滤液I溶质的成分是。
,滤液I溶质的成分是。