题目内容
7.有下列物质:①CaCl2 ②PH3 ③H2O2 ④Na2O2 ⑤KOH ⑥(NH4)2SO4 ⑦F2(答题填编号)(1)含有离子键的物质①④⑤⑥,含有非极性键的离子化合物④;
(2)含有极性键的物质②③⑤⑥;
(3)含有非极性键的共价化合物③.
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,同种非金属元素之间易形成非极性键,不同非金属元素之间易形成极性键,含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,只含共价键的化合物是共价化合物,据此分析解答.
解答 解:①CaCl2中钙离子和氯离子之间只存在离子键,属于离子化合物;
②PH3分子中P-H原子之间只存在极性键,属于共价化合物;
③H2O2分子中H-O原子之间存在极性键、O-O原子之间存在非极性键,属于共价化合物;
④Na2O2中钠离子和过氧根离子之间存在离子键、O-O原子之间存在非极性键,属于离子化合物;
⑤KOH中钾离子和氢氧根离子之间存在离子键、O-H原子之间存在极性键,属于离子化合物;
⑥(NH4)2SO4中铵根离子和硫酸根离子之间存在离子键、N-H与之间存在极性键、S-O原子之间存在极性键,所以属于离子化合物;
⑦F2中F-F原子之间只存在非极性键,属于单质,
(1)含有离子键的物质①④⑤⑥,含有非极性键的离子化合物④,故答案为:①④⑤⑥;④;
(2)含有极性键的物质②③⑤⑥,故答案为:②③⑤⑥;
(3)含有非极性键的共价化合物③,故答案为:③.
点评 本题考查化学键和化合物的关系,明确物质构成微粒及物质之间作用力即可解答,注意铵盐中都含有配位键,配位键属于共价键.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
17.某元素的一种核素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子,在a g HmX分子中含质子的物质的量是( ) mol.
| A. | $\frac{a}{A+m}$(A-N+m) | B. | $\frac{a}{A}$(A-N) | C. | $\frac{a}{A+m}$(A-N) | D. | $\frac{a}{A}$(A-N+m) |
18.下列反应的离子方程式正确的是( )
| A. | 钠与水的反应:Na+H2O=Na++OH-+H2↑ | |
| B. | 氯气与水反应:Cl2+H2O=2H++Cl-+ClO- | |
| C. | 用FeCl3溶液腐蚀印刷电路板:Fe++Cu=Fe2++Cu2+ | |
| D. | 氢氧化铝中和胃酸:Al(OH)3+3H+=Al3++3H2O |
2.下列关于元素周期表和元素周期律的说法错误的是( )
| A. | 因为K比Na容易失去电子,所以K比Na的还原性强 | |
| B. | 第二周期元素从Li到F,非金属性逐渐增强 | |
| C. | 在金属和非金属的分界线处,可以找到用于作催化剂的元素 | |
| D. | O与S为同主族元素,且O比S的非金属性强 |
16.某溶液与金属铝反应能放出氢气,则在该溶液中一定能大量共存的离子组是( )
| A. | NH4+、NO3-、CO32-、Na+ | B. | Na+、I-、Cl-、SO42- | ||
| C. | NO3-、Fe3+、Cl-、I- | D. | NO3-、Cl-、Na+、SO32- |
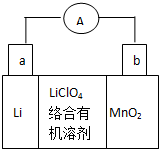 锂锰电池的体积小,性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO2晶格中,
锂锰电池的体积小,性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO2晶格中, CO(g)+H2(g)当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g)当增加反应物物质的量时,平衡一定向正反应方向移动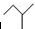 表示2-甲基丁烷,则
表示2-甲基丁烷,则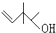 所表示的有机物的分子式为C7H14O,该物质的官能团有碳碳双键和羟基.
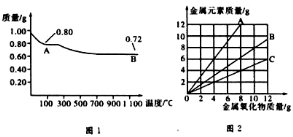
所表示的有机物的分子式为C7H14O,该物质的官能团有碳碳双键和羟基. O和Cu2O。某学习小组取0.98g(用精密天平测量)Cu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图1所示:另外,某同学绘制了三条表示金属氧化物与其所含金属元素的质量的关系曲线,如图2所示。则下列分析正确的是
O和Cu2O。某学习小组取0.98g(用精密天平测量)Cu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图1所示:另外,某同学绘制了三条表示金属氧化物与其所含金属元素的质量的关系曲线,如图2所示。则下列分析正确的是