题目内容
(本题共12分)
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:


完成下列填空:
33.在a中加入15 mL苯和少量铁屑。在b中小心加入4.0 mL 液态溴。向a中滴入几滴溴,有白雾产生,是因为生成了 气体。继续滴加至液溴滴完。装置d的作用是__________。
34.液溴滴完后,经过下列步骤分离提纯:①向a中加入10 mL水,然后过滤除去未反应的铁屑;②滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是_____________;③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_____________。
35.经过上述分离操作后,粗溴苯中还含有的主要杂质为 ,要进一步提纯,下列操
作中必须的是________(填写字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
36.在该实验中,a的容积最适合的是 (填写字母)。
A.25 mL B.50 mL C.250 mL D.500 mL
(共12分)33.HBr ;吸收HBr和Br2(2分)34.除去未反应的Br2(2分);干燥(2分);
35.苯 ;C(2分);36.B(2分)。
【解析】
试题分析:33.在铁作催化剂时苯和液态溴发生取代反应产生溴苯和HBr,HBr容易挥发,遇到空气中的水蒸气形成氢溴酸的小液滴,产生白雾产生。继续滴加至液溴滴完。由于HBr、Br2都是大气污染物,为了防止大气污染,同时避免引起倒吸现象的反应,用NaOH溶液吸收产生的HBr及为反应挥发的溴蒸气。故装置d的作用是吸收HBr和Br2;
34.液溴滴完后,经过下列步骤分离提纯:①向a中加入10 mL水,然后过滤除去未反应的铁屑;②滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是除去未反应的Br2;③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是吸收水分或干燥溴苯;
35.经过上述分离操作后,粗溴苯中还含有的主要杂质为未反应的苯,由于苯、溴苯是互溶的沸点不同的液体混合物,所以要进一步提纯,必须操作是蒸馏;
36.在该实验中,向烧瓶中加入的液体物质的体积是15 mL+ 4.0 mL=19ml。由于液体混合物加热时液体的体积占容器容积的1/3——2/3。所以a的容积最适合的是50 mL,选项是B。
考点:考查反应现象的原因分析、物质的性质及作用、混合物的分离方法、仪器的选择使用的知识。

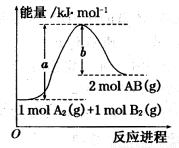
 键的物质的量为 。
键的物质的量为 。

 3NH3↑+8AlO2-
3NH3↑+8AlO2-