题目内容
3.选择下列实验方法分离物质,将分离方法的序号填在横线上.A、加热分解 B、结晶法 C、分液法 D、蒸馏法 E、过滤法 F、萃取法
(1)E分离饱和食盐水和沙子的混合物
(2)B从硝酸钾和氯化钠的混合溶液中获得硝酸钾(溶解度差异很大)
(3)C分离水和汽油的混合物
(4)D分离四氯化碳(沸点为76.75°C)和甲苯(沸点为110.6°C)
(5)F从碘水中提取碘.
分析 (1)沙子不溶于水;
(2)硝酸钾和氯化钠的溶解度受温度影响不同;
(3)水和汽油不分层;
(4)二者互溶,但沸点不同;
(5)碘不易溶于水,易溶于有机溶剂.
解答 解:(1)沙子不溶于水,则选择过滤法分离,故答案为:E;
(2)硝酸钾和氯化钠的溶解度受温度影响不同,则选择结晶法分离,故答案为:B;
(3)水和汽油不分层,则选择分液法分离,故答案为:C;
(4)二者互溶,但沸点不同,则选择蒸馏法分离,故答案为:D;
(5)碘不易溶于水,易溶于有机溶剂,则选择萃取法分离,故答案为:F.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意分离方法的选择,题目难度不大.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案
相关题目
13.保存下列物质的方法正确是( )
| A. | 氢氟酸保存在用塑料盖的玻璃瓶中 | |
| B. | 稀硫酸可以用铁桶贮存 | |
| C. | 氯水盛放在棕色的玻璃瓶中 | |
| D. | 水玻璃保存在带有玻璃塞的玻璃瓶中 |
11.密闭容器中自由移动的活塞两边分别充入空气和H2、O2的混合气体,开始体积比为1:3,若将H2、O2的混合气体点燃引爆,恢复到原来温度(水为液态),活塞右滑停留于容器的正中央,则原来H2、O2的体积比可能为( )
| A. | 2:7 | B. | 5:4 | C. | 1:1 | D. | 7:2 |
18.下列实验或叙述不符合绿色化学理念的是( )
| A. | 制CuSO4时先将Cu氧化成CuO后再与稀硫酸反应 | |
| B. | 采用银作催化剂,乙烯和氧气制取环氧乙烷,原子利用率100% | |
| C. | 用乙醇代替汽油作汽车燃料 | |
| D. | 用稀硝酸和铜制取Cu(NO3)2 |
8.下列物质间的转化在给定条件下能实现的是( )
| A. | Cu$→_{△}^{O_{2}}$CuO$\stackrel{H_{2}O}{→}$Cu(OH)2 | |
| B. | Fe2O3$\stackrel{盐酸}{→}$FeCl3溶液$\stackrel{NaOH、过滤、加热}{→}$Fe2O3 | |
| C. | Mg(OH)2$\stackrel{盐酸}{→}$MgCl2(aq)$\stackrel{电解}{→}$Mg | |
| D. | Na$→_{△}^{O_{2}}$Na2O$\stackrel{CO_{2}}{→}$Na2CO3 |
15.下列说法正确的是( )
| A. | 有质子的微粒一定有中子 | |
| B. | 通常所说的氢元素是指${\;}_{1}^{1}$H | |
| C. | 16O中的“16”表示氧元素的近似相对原子质量 | |
| D. | 根据反应K35ClO3+6H37Cl=KCl+3Cl2↑+3H2O得到的Cl2,其相对分子质量为73.3 |
4.在标准状况时mg某气体X的体积为VL,其摩尔质量为M g/mol,阿伏加德罗常数为NA,则下列有关该气体的说法不正确的是( )
| A. | M/NA表示该气体单个分子的质量 | B. | mNA/M表示该气体的分子数 | ||
| C. | M/22.4表示该气体的密度 | D. | VM/mNA表示该气体一个分子的体积 |
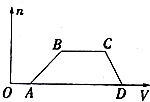 某混合溶液中可能含有H2SO4、MgCl2、Al2(SO4)3、NH4Cl、NaCl中的几种物质,往该溶液中逐渐加入NaOH溶液,产生沉淀的物质的量(n)与加入的NaOH溶液体积(V)的关系如图所示.回答下列问题:
某混合溶液中可能含有H2SO4、MgCl2、Al2(SO4)3、NH4Cl、NaCl中的几种物质,往该溶液中逐渐加入NaOH溶液,产生沉淀的物质的量(n)与加入的NaOH溶液体积(V)的关系如图所示.回答下列问题: