题目内容
下列离子方程式正确的是( )
| A、0.01mol/L NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液等体积混合NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3?H2O | ||||
| B、Na2O2加入H218O中:2Na2O2+2H218O=4Na++4OH-+18O2↑ | ||||
C、NH4HCO3溶液与过量NaOH溶液共热:NH4++OH-
| ||||
D、浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+
|
考点:离子方程式的书写
专题:离子反应专题
分析:A.氢氧根离子先和一水合氨反应、然后铝离子反应,二者的物质的量之比为1:2,所以二者反应生成硫酸钡、氢氧化铝沉淀和一水合氨;
B.水中的O氧元素生成氢氧根离子,且过氧根离子中的O元素一半生成氢氧根离子、一半生成氧气;
C.二者反应生成碳酸钠、水和氨气;
D.硝酸与过量Fe反应得到的是Fe2+.
B.水中的O氧元素生成氢氧根离子,且过氧根离子中的O元素一半生成氢氧根离子、一半生成氧气;
C.二者反应生成碳酸钠、水和氨气;
D.硝酸与过量Fe反应得到的是Fe2+.
解答:
解:A.氢氧根离子先和一水合氨反应、然后和铝离子反应,二者的物质的量之比为1:2,所以二者反应生成硫酸钡、氢氧化铝沉淀和一水合氨,离子方程式为NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3?H2O,故A正确;
B.水中的O氧元素生成氢氧根离子,且过氧根离子中的O元素一半生成氢氧根离子、一半生成氧气,离子方程式为2Na2O2+2H218O=4Na++2OH-+218OH-+O2↑,故B错误;
C.二者反应生成碳酸钠、水和氨气,离子方程式为NH4++HCO3-+2OH-
NH3↑+CO32-+H2O,故C错误;
D.硝酸与过量Fe反应得到的是Fe2+,离子方程式为Fe+2NO3-+4H+
Fe2++2NO2↑+2H2O,故D错误;
故选A.
B.水中的O氧元素生成氢氧根离子,且过氧根离子中的O元素一半生成氢氧根离子、一半生成氧气,离子方程式为2Na2O2+2H218O=4Na++2OH-+218OH-+O2↑,故B错误;
C.二者反应生成碳酸钠、水和氨气,离子方程式为NH4++HCO3-+2OH-
| ||
D.硝酸与过量Fe反应得到的是Fe2+,离子方程式为Fe+2NO3-+4H+
| ||
故选A.
点评:本题考查离子方程式正误判断,为高考高频点,明确物质的性质及离子反应条件是解本题关键,易错选项是AB,注意A中反应物的量关系、注意B中过氧根离子的生成物,为易错点.

练习册系列答案
相关题目
阿司匹林是一种常用的解热镇痛药,其结构简式如图,其不可能有的性质为( )
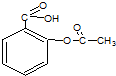

| A、该物质可以与氢气发生加成 |
| B、该物质能发生酯化反应 |
| C、该物质可水解生成水杨酸 |
| D、该物质极易溶于水和有机溶剂 |
下列有关蛋白质的叙述中,不正确的是( )
| A、蛋白质溶液中加入饱和(NH4)2SO4溶液,蛋白质析出,再加水也不溶解 |
| B、人工合成的具有生命活性的蛋白质-结晶牛胰岛素是1965年我国科学家最先合成的 |
| C、重金属盐能使蛋白质变性,所以误食重金属盐会中毒 |
| D、浓HNO3溅在皮肤上,使皮肤呈黄色,是由于浓HNO3和蛋白质发生颜色反应 |
一定条件下进行反应:COCl2(g)?Cl2(g)+CO(g),向2.0L恒容密闭容器中充入1.0 mol COCl2(g),经过一段时间后达到平衡.反应过程中测得的有关数据见下表:
下列说法正确的是( )
| t/s | 0 | 2 | 4 | 6 | 8 |
| n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
| A、A、保持其他条件不变,升高温度,平衡时c(Cl2)=0.22 mol?L-1,则反应的△H<0 |
| B、若在2 L恒容绝热(与外界没有热量交换)密闭容器进行该反应,化学平衡常数不变 |
| C、保持其他条件不变,起始向容器中充入1.2 molCOCl2、0.60 molCl2和0.60 molCO,反应达到平衡前的速率:v(正)<v(逆) |
| D、保持其他条件不变,起始向容器中充入1.0 molCl2和0.8 molCO,达到平衡时,Cl2的转化率小于60% |
下列关于实验现象的描述不正确的是( )
| A、把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| B、用锌片做阳极,铁片做阴极,电解氯化铜溶液,铁片表面析出铜 |
| C、把铜片插入三氯化铁溶液,在铜片表面析出铁 |
| D、把锌放入稀盐酸中,加几滴氯化铜溶液,产生气泡速率加快 |
水是人类赖以生存的重要物质,水污染却严重影响着人类的生存环境.目前,水污染主要来自 ( )
①工业生产中废渣、废液的任意排放
②农业生产中农药、化肥的过量使用
③城市生活污水的任意排放
④生活垃圾和废旧电池的随意丢弃.
①工业生产中废渣、废液的任意排放
②农业生产中农药、化肥的过量使用
③城市生活污水的任意排放
④生活垃圾和废旧电池的随意丢弃.
| A、①② | B、②③④ |
| C、①③④ | D、①②③④ |
下列化学方程式改写成离子方程式不正确的是( )
| A、CuCl2+2NaOH═Cu(OH)2↓+2NaCl;Cu2++20H═Cu(OH)2↓ |
| B、BaSO4+2HCl═BaCl2+CO2↑+H2O;SO42-+2H+═CO2↑+H2O |
| C、Ca(NO3)2+Na2CO3═CaCO3↓+2NaNO3 Ca2++CO32-═CaCO3↓ |
| D、2KOH+H2SO4═K2SO4+2H2O;H++OH-═H2O |
NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A、常温常压下,8gO2和O3的混合物含有2AA个电子 |
| B、29gC4H10中含有的共价键个数为13NA |
| C、1L1 moI?L-1的NaClO溶液中含有ClO的数日为NA |
| D、标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.2NA |
