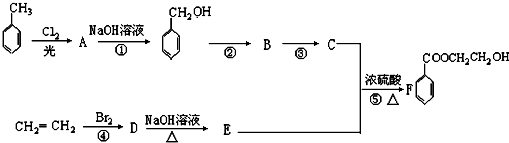
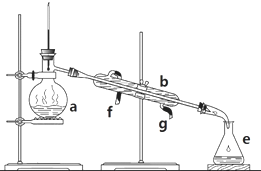
题目内容
阿司匹林是一种常用的解热镇痛药,其结构简式如图,其不可能有的性质为( )
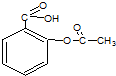

| A、该物质可以与氢气发生加成 |
| B、该物质能发生酯化反应 |
| C、该物质可水解生成水杨酸 |
| D、该物质极易溶于水和有机溶剂 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:由结构简式可知,含苯环、-COOH、-COOC-,结合羧酸、酯的性质来解答.
解答:
解:A.含苯环,可与氢气发生加成反应,故A正确;
B.含-COOH,可发生酯化反应,故B正确;
C.含-COOC-可水解生成邻羟基苯甲酸(水杨酸),故C正确;
D.该物质属于酯类,不溶于水,易溶于有机溶剂,故D错误;
故选D.
B.含-COOH,可发生酯化反应,故B正确;
C.含-COOC-可水解生成邻羟基苯甲酸(水杨酸),故C正确;
D.该物质属于酯类,不溶于水,易溶于有机溶剂,故D错误;
故选D.
点评:本题考查有机物的结构与性质,为高考常见题型,把握常见有机物的官能团为解答的关键,熟悉酯、羧酸的性质即可解答,题目难度不大.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
只用一种试剂就能将NH4Cl、NaCl、AlCl3、MgCl2四种无色透明溶液区别出来,这种试剂可以是( )
| A、氨水 | B、氯化钙溶液 |
| C、氢氧化钠溶液 | D、稀硫酸 |
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A、1 L 0.1 mol?L-1 (NH4)2Fe(SO4)2?6H2O溶液中:c(NH4+)+c(Fe2+)+c(H+)=c(OH-)+c(SO42-) |
| B、0.1 mol?L-1的NH4Cl与0.1 mol?L-1的NH3?H2O等体积混合:c(NH4+)+2c(H+)=c(NH3?H2O)+2c(OH-) |
| C、pH=9.4、浓度均为0.1 mol?L-1的HCN与NaCN的混合溶液中:c(Na+)>c(CN-)>c(HCN)>c(OH-) |
| D、0.1 mol?L-1 CH3COONa 溶液与0.05 mol?L-1盐酸等体积混合后的酸性溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
下列离子方程式正确的是( )
| A、0.01mol/L NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液等体积混合NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3?H2O | ||||
| B、Na2O2加入H218O中:2Na2O2+2H218O=4Na++4OH-+18O2↑ | ||||
C、NH4HCO3溶液与过量NaOH溶液共热:NH4++OH-
| ||||
D、浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+
|
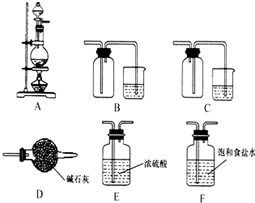 A、B、C、D、E均为短周期主族元素,其原子序数依次增大.其中A元素原子核内只有1个质子;A与C,B与D分别同主族; B、D两元素原子序数之和是A、C两元素原子序数之和的2倍.
A、B、C、D、E均为短周期主族元素,其原子序数依次增大.其中A元素原子核内只有1个质子;A与C,B与D分别同主族; B、D两元素原子序数之和是A、C两元素原子序数之和的2倍.