题目内容
水溶液中能大量共存的一组离子是( )
| A、K+、Ca2+、Cl-、NO3- |
| B、H+、Fe2+、SO42-、ClO- |
| C、Na+、Fe3+、Cl-、CO32- |
| D、K+、NH4+、OH-、SO42- |
考点:离子共存问题
专题:
分析:离子之间不反应生成气体、沉淀、弱电解质、络合物或发生双水解反应、氧化还原反应的就能共存,以此解答该题.
解答:
解:A.离子之间不发生任何反应,可大量共存,故A正确;
B.H+、Fe2+、ClO-发生氧化还原反应而不能大量共存,故B错误;
C.Fe3+、CO32-发生互促水解反应而不能大量共存,故C错误;
D.NH4+、OH-反应生成一水合氨而不能大量共存,故D错误.
故选A.
B.H+、Fe2+、ClO-发生氧化还原反应而不能大量共存,故B错误;
C.Fe3+、CO32-发生互促水解反应而不能大量共存,故C错误;
D.NH4+、OH-反应生成一水合氨而不能大量共存,故D错误.
故选A.
点评:本题考查离子共存,为高考热点,明确离子共存条件是解本题关键,常常与盐类水解、氧化还原反应、离子颜色、pH等联合考查,题目难度中等.

练习册系列答案
相关题目
在298K、1.01×105 Pa下,将22g CO2通入1mol?L-1 NaOH溶液750mL中充分反应,测得反应放出x kJ的热量.已知在该条件下,1mol CO2 通入2mol?L-1 NaOH溶液1L中充分反应放出y kJ的热量.则CO2与NaOH溶液反应生成NaHCO3的热化学方程式正确的是( )
| A、CO2(g)+NaOH(aq)═NaHCO3 (aq)△H=-(2y-x) kJ?mol-1 |
| B、CO2(g)+NaOH(aq)═NaHCO3 (aq)△H=-(2x-y) kJ?mol-1 |
| C、CO2(g)+NaOH(aq)═NaHCO3 (aq)△H=-(4x-y) kJ?mol-1 |
| D、2CO2(g)+2NaOH(l)═2NaHCO3 (l)△H=-(8x-2y) kJ?mol-1 |
工业上以铬铁矿(主要成分为FeO?Cr2O3)、碳酸钠、氧气、和硫酸为原料生产重铬酸钠(Na2Cr2O7?2H2O),其主要反应为:下列说法正确的是( )
(1)4FeO?Cr2O3+8Na2CO3+7O2
8Na2CrO4+2Fe2O3+8CO2
(2)2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2O.
(1)4FeO?Cr2O3+8Na2CO3+7O2
| ||
(2)2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2O.
| A、反应(1)和(2)均为氧化还原反应 |
| B、反应(1)的氧化剂是O2,还原剂是FeO?Cr2O3 |
| C、高温下,O2的氧化性强于Fe2O3,弱于Na2CrO4 |
| D、反应(1)中每生成1molNa2CrO4时电子转移3mol |
 如图所示的 甲、乙、丙三种物质,含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
如图所示的 甲、乙、丙三种物质,含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )①C ②H2O2 ③Na ④Fe ⑤HNO3.
| A、①③④ | B、①②⑤ |
| C、①②③⑤ | D、①②③④⑤ |
用惰性电极电解下列物质的水溶液,一段时间后(温度不变),再加入一定质量的另一种物质(括号内物质),溶液能恢复到与电解前的溶液完全一样的是( )
| A、CuCl2(CuO) |
| B、NaOH(Na2O) |
| C、NaCl(NaCl) |
| D、H2SO4(H2O) |

 的芳香族化合物的同分异构体有
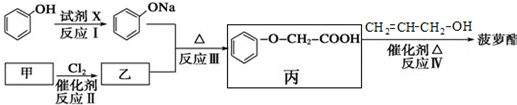
的芳香族化合物的同分异构体有 由甲苯及其它必要物质经如下步骤也可合成B:
由甲苯及其它必要物质经如下步骤也可合成B: 反应Ⅰ的试剂及条件为
反应Ⅰ的试剂及条件为