题目内容
4.在下列各溶液中,离子可能大量共存的是( )| A. | 无色的碱性溶液中:CrO42-、K+、Na+、SO42- | |
| B. | 含有大量ClO-的溶液中:K+、H+、I-、SO42 | |
| C. | -使pH试纸变红的溶液中:NH4+、Na+、SO42-、Cl- | |
| D. | 水电离产生的c(H+)=10-12mol•L-1的溶液中:Na+、Fe2+、SO42-、NO3- |
分析 A.重铬酸跟离子为有色离子;
B.次氯酸根离子与氢离子、碘离子反应;
C.使pH变红的溶液中存在大量氢离子,四种离子之间不反应,都不与氢氧根离子反应;
D.水电离产生的c(H+)=10-12mol•L-1的溶液中存在大量氢离子或氢氧根离子,亚铁离子与氢氧根离子反应,硝酸根离子在酸性条件下能够氧化亚铁离子.
解答 解:A.CrO42-为有色离子,在溶液中不能存在,故A错误;
B.ClO-与H+、I-发生反应,在溶液中不能大量共存,故B错误;
C.使pH试纸变红的溶液呈碱性,溶液中存在大量氢氧根离子,NH4+、Na+、SO42-、Cl-之间不发生反应,都不与氢氧根离子反应,在溶液中能够大量共存,故C正确;
D.水电离产生的c(H+)=10-12mol•L-1的溶液为酸性或碱性溶液,Fe2+、NO3-在酸性条件下发生氧化还原反应,Fe2+与碱性溶液中的氢氧根了反应,在溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
11.在室温下,0.1mol•L-1100ml 的醋酸溶液中,欲使其溶液的c(H+)增大,但又要使醋酸电离程度减少,应采取( )
| A. | 加入少量CH3COONa固体 | B. | 通入少量氯化氢气体 | ||
| C. | 提高温度 | D. | 加入少量纯醋酸 |
12.相对分子质量为86的某烃M,其分子中含有4个甲基,则A的一氯代物(不考虑立体异构)最多有( )
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
13.下列有关工业生产的叙述正确的是( )
| A. | 合成氨生产中将NH3液化分离,虽可提高N2、H2的转化率但减小了反应速率 | |
| B. | 硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量 | |
| C. | 电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的C12进入阳极室 | |
| D. | 侯氏制碱法是将氨气和二氧化碳先后通入饱和氯化钠溶液中,制得碳酸氢钠固体,再在高温下灼烧,转化为碳酸钠固体 |
14.下列图示实验合理的是( )
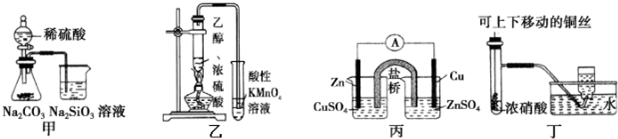

| A. | 图甲证明非金属性强弱:S>C>Si | |
| B. | 装置乙可用于检验有乙烯生成 | |
| C. | 图丙构成铜锌原电池,产生持续稳定的电流 | |
| D. | 图丁可制备并收集NO2气体 |
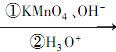 RCOOH+R1COOH
RCOOH+R1COOH .
.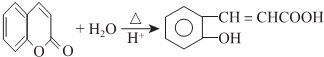 .
.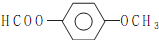 .
.