题目内容
15.以乙烯为原料合成化合物C的流程如图所示: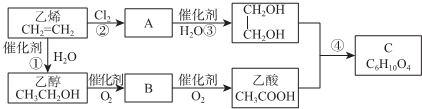
已知:CH3CH2Cl+H2O$→_{△}^{催化剂}$CH3CH2OH+HCl
(1)乙醇和乙酸中所含官能团的名称分别为:羟基和羧基.
(2)B物质的结构简式为CH3CHO.
(3)①、③、④的反应类型分别为加成、水解或取代、酯化或取代反应.
(4)反应④的化学方程式为:HOCH2CH2OH+2CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH3+2H2O.
分析 CH2=CH2与Cl2发生加成反应生成物质A:ClCH2CH2Cl,ClCH2CH2Cl水解生成HOCH2CH2OH;CH2=CH2与H2O反应生成CH3CH2OH,CH3CH2OH发生催化氧化得到物质B:CH3CHO,CH3CHO氧化得到CH3COOH,CH3COOH与HOCH2CH2OH在浓硫酸条件下发生酯化反应生成CH3COOCH2CH2COOCH3,结合题目分析解答.
解答 解:CH2=CH2与Cl2发生加成反应生成物质A:ClCH2CH2Cl,ClCH2CH2Cl水解生成HOCH2CH2OH;CH2=CH2与H2O反应生成CH3CH2OH,CH3CH2OH发生催化氧化得到物质B:CH3CHO,CH3CHO氧化得到CH3COOH,CH3COOH与HOCH2CH2OH在浓硫酸条件下发生酯化反应生成CH3COOCH2CH2COOCH3,
(1)乙醇和乙酸中所含官能团的名称分别为羟基、羧基,故答案为:羟基;羧基;
(2)通过以上分析知,B结构简式为CH3CHO,故答案为:CH3CHO;
(3)①、③、④的反应类型分别为加成反应、水解反应或取代反应、酯化反应或取代反应,
故答案为:加成反应;水解(取代)反应;酯化(取代);
(4)乙酸和乙二醇发生酯化反应生成乙酸乙二酯,反应方程式为HOCH2CH2OH+2CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH3+2H2O,
故答案为:HOCH2CH2OH+2CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH3+2H2O.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析判断能力,明确有机物官能团及其性质关系是解本题关键,根据某些物质结构简式、反应条件进行推断,题目难度不大.

| A. | BaSO4的水溶液不导电,故BaSO4是弱电解质 | |
| B. | 甲烷、甲醛、甲酸都不存在同分异构体,则甲醚(CH3OCH3)也不存在同分异构体 | |
| C. | 反应2Mg(s)+CO2(g)═C(s)+2MgO(s)能自发进行,则该反应的△H>0 | |
| D. | AgCl在同温、同浓度的CaCl2和NaCl溶液中的溶解度不同 |
 某学生欲用已知物质的量浓度的盐酸去测定在空气中露置一段时间后的NaOH固体的纯度.设计如下方案:
某学生欲用已知物质的量浓度的盐酸去测定在空气中露置一段时间后的NaOH固体的纯度.设计如下方案:①称取W g样品,准确配成500mL溶液.
②准确配制0.1000mol/L的标准盐酸.
③用滴定管取所配制碱液25.00mL于锥形瓶,并向瓶中滴几滴甲基橙试液.
④向锥形瓶中逐滴滴入标准盐酸,直到终点.
⑤记录数据,计算.请回答:
(1)在①操作中要使用的定量的玻璃仪器是500ml容量瓶.
(2)操作④装标准盐酸的滴定管是酸式滴定管.
(3)滴定过程中左手控制酸式滴定管的活塞,右手向一个方向摇动锥形瓶.眼睛应始终注视锥形瓶内溶液的颜色变化,判断滴定到达终点的现象是滴加最后一滴盐酸,溶液的颜色由黄色变为橙色,且在半分钟内不变色.
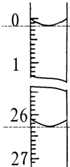
(4)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为26.10ml.
(5)某学生根据3次实验分别记录有关数据如表:
| 滴定 次数 | 待测NaOH溶液的体积/mL | 0.1000mol/L盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 平均耗用盐酸 体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.15 | ①V=26.20 |
| 第二次 | 25.00 | 0.56 | 30.30 | |
| 第三次 | 25.00 | 0.20 | 26.45 | |
③根据上面结果计算NaOH的纯度$\frac{2.096}{W}$×100%.
(6)下列操作中,可能使测定结果偏低的是ACF.
A.称取样品时,样品和砝码位置放反了
B.配制标准盐酸过程中,读取量筒读数时,俯视刻度线
C.碱式滴定管清洗后,未用待测液润洗
D.酸式滴定管清洗后,未用待测液润洗
E.锥形瓶装液前未干燥,有水珠附着在瓶壁
F.读取酸式滴定管读数时,第一次读数仰视,第二次读数俯视.
| A. | 向某物质中滴加盐酸后,有能使澄清石灰水变浑浊的无色无味气体产生,证明含CO32- | |
| B. | 将某化合物进行焰色实验,透过蓝色钴玻璃观察,焰色为紫色,证明含钾 | |
| C. | 待检液逐滴加入NaOH溶液,有白色胶状沉淀产生,后来沉淀逐渐消失,则原溶液中可能含有Al3+ | |
| D. | 待检液中先加入KSCN溶液,无明显现象,再加入氯水,溶液显血红色,则待检液中一定含有Fe2+ |
| A. | 一定条件下,将1 mol N2和3 mol H2混合发生反应,转移的电子总数为6 NA | |
| B. | 1 L 0.1 mol•L-1的Na2CO3溶液中阴离子的总数大于0.1 NA | |
| C. | 标准状况下,44.8LHF中含有分子的数目为2NA | |
| D. | 1 mol-CH3中所含的电子总数为10 NA |
| A. | CO2通入到 CaCl2溶液中 | |
| B. | NH3通入 AlCl3溶液中 | |
| C. | 用脱脂棉包裹Na2O2粉末向其中通入适量二氧化碳 | |
| D. | 稀盐酸滴加到Fe(OH)3胶体中 |
| A. | 无色的碱性溶液中:CrO42-、K+、Na+、SO42- | |
| B. | 含有大量ClO-的溶液中:K+、H+、I-、SO42 | |
| C. | -使pH试纸变红的溶液中:NH4+、Na+、SO42-、Cl- | |
| D. | 水电离产生的c(H+)=10-12mol•L-1的溶液中:Na+、Fe2+、SO42-、NO3- |
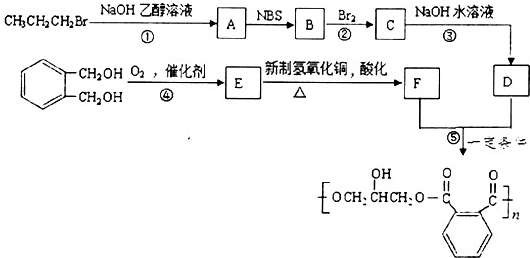
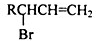
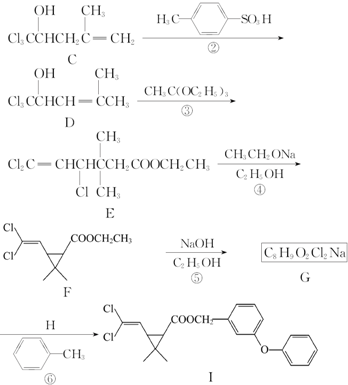
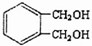 的同分异构体中同时符合下列条件的芳香族化合物,试写出其中一种的结构简式
的同分异构体中同时符合下列条件的芳香族化合物,试写出其中一种的结构简式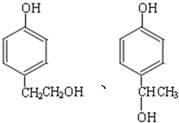 (其中之一);
(其中之一);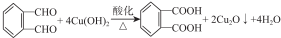 ;
;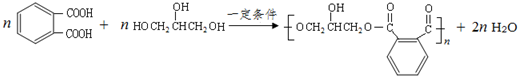 .
.
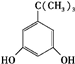 、
、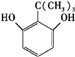 、
、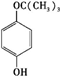 任意一种.
任意一种.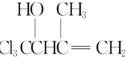 为原料合成
为原料合成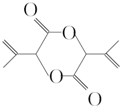 (用合成路线流程图表示,并注明反应条件).
(用合成路线流程图表示,并注明反应条件).