题目内容
17.下列分子中,属于含有非极性键的分子是( )| A. | H2O | B. | Cl2; | C. | CCl4; | D. | CO2 |
分析 同种非金属元素之间形成非极性共价键,不同非金属元素之间形成极性共价键,以此来解答.
解答 解:A.水的结构式为H-O-H,水中存在两个氧氢键,不含非极性键,故A错误;
B.氯气的结构式为:Cl-Cl,氯气中存在1对氯氯共用电子对,为非极性键,故B正确;
C.C形成4个共价键,CCl4中存在4对碳氯共用电子对,结构式为 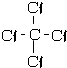 ,为极性键,故C错误;
,为极性键,故C错误;
D.二氧化碳中存在2个碳氧双键,其结构式为O=C=O,为极性键,故D错误.
故选B.
点评 本题考查了非极性共价键和极性共价键的判断,根据概念的内涵来分析解答,注意极性共价键为不同非金属元素之间形成的共价键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8. 如图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录,其中描述合理的组合是( )
如图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录,其中描述合理的组合是( )
①Zn为正极,Cu为负极 ②H+向负极移动
③电子是由Zn经外电路流向Cu ④Cu极上有H2产生
⑤若有1mol电子流过导线,则产生的H2为0.5mol
⑥正极的电极反应式为Zn-2e-═Zn2+.
 如图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录,其中描述合理的组合是( )
如图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录,其中描述合理的组合是( )①Zn为正极,Cu为负极 ②H+向负极移动
③电子是由Zn经外电路流向Cu ④Cu极上有H2产生
⑤若有1mol电子流过导线,则产生的H2为0.5mol
⑥正极的电极反应式为Zn-2e-═Zn2+.
| A. | ①②③ | B. | ③④⑤ | C. | ④⑤⑥ | D. | ②③④ |
2.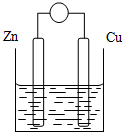 原电池是将化学能转变成电能的装置.原电池结构示意图(以Zn-Cu-稀H2SO4原电池为例)铜片和锌片作电极,稀硫酸做电解质溶液.
原电池是将化学能转变成电能的装置.原电池结构示意图(以Zn-Cu-稀H2SO4原电池为例)铜片和锌片作电极,稀硫酸做电解质溶液.
填表:
【注意】①电解质溶液的pH增大
②在同一个电池中两极反应时,“失去电子数”与“得到电子数”要相同.
(3)原电池工作时电子、离子运动方向.
①外电路(导线):电子从负极经导线流向正极
②原电池内电解质溶液中:阴离子流向负极,阳离子流向正极.
 原电池是将化学能转变成电能的装置.原电池结构示意图(以Zn-Cu-稀H2SO4原电池为例)铜片和锌片作电极,稀硫酸做电解质溶液.
原电池是将化学能转变成电能的装置.原电池结构示意图(以Zn-Cu-稀H2SO4原电池为例)铜片和锌片作电极,稀硫酸做电解质溶液.填表:
| 电极 | 电极材料 | 电极反应式 | 反应类型 |
| 正极 | |||
| 负极 | |||
| 总反应式 | |||
②在同一个电池中两极反应时,“失去电子数”与“得到电子数”要相同.
(3)原电池工作时电子、离子运动方向.
①外电路(导线):电子从负极经导线流向正极
②原电池内电解质溶液中:阴离子流向负极,阳离子流向正极.
6.下列说法正确的是( )
| A. | 为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 | |
| B. | 热的浓盐酸可以除去试管内残留的MnO2 | |
| C. | 在未知溶液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液中存在SO42-或SO32- | |
| D. | 施肥时,草木灰(有效成分为K2CO3)与NH4Cl混合使用,可以同时提供K、N两种有效成分 |
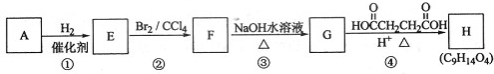
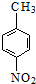 $\stackrel{KMnO_{4}/H+}{→}$[A]$→_{浓H_{2}SO_{4}/△}^{CH_{3}CH_{2}OH}$[B]$→_{(还原)}^{Fe/H+}$
$\stackrel{KMnO_{4}/H+}{→}$[A]$→_{浓H_{2}SO_{4}/△}^{CH_{3}CH_{2}OH}$[B]$→_{(还原)}^{Fe/H+}$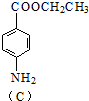
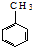 $→_{H+}^{KMnO_{4}}$
$→_{H+}^{KMnO_{4}}$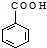 ②
②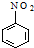 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$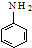
 、B
、B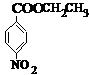 .用1H核磁共振谱可以证明化合物B中有4种氢处于不同的化学环境.
.用1H核磁共振谱可以证明化合物B中有4种氢处于不同的化学环境.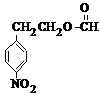 、
、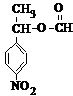 .
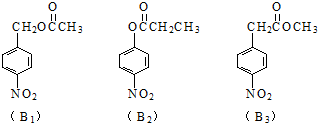
.
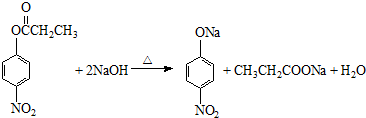 .
.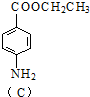 $\stackrel{H_{2}O/OH-}{→}$ $\stackrel{H+}{→}$[D]+C2H5OH
$\stackrel{H_{2}O/OH-}{→}$ $\stackrel{H+}{→}$[D]+C2H5OH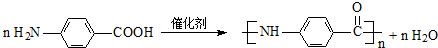 .
. .
.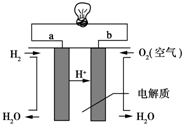 人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.
人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.