题目内容
7. 人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.
人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4═2PbSO4+2H2O.正极电极反应式为PbO2+4H++SO42-+2e-═PbSO4+2H2O.
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu═2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为Cu,当线路中转移0.2mol电子时,则被腐蚀铜的质量为6.4g.
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为B.
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
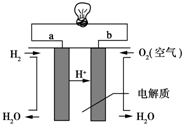
(4)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:
①氢氧燃料电池的总反应化学方程式是:2H2+O2=2H2O.
②电池工作一段时间后硫酸溶液的浓度减小(填“增大”、“减小”或“不变”).
分析 (1)放电时,正极上PbO2得电子;
(2)该电池反应中,铜失电子发生氧化反应,作负极;根据电极方程式计算;
(3)原电池中失电子的一极为负极;
(4)①氢氧燃料电池的总反应即是氢气与氧气反应生成水;
②根据燃料电池的总反应方程式判断硫酸浓度的变化.
解答 解:(1)放电时,正极上PbO2得电子,正极反应式为PbO2+4H++SO42-+2e-═PbSO4+2H2O,
故答案为:PbO2+4H++SO42-+2e-═PbSO4+2H2O;
(2)该电池反应中,铜失电子发生氧化反应,作负极;负极反应式为Cu-2e-=Cu2+,则当线路中转移0.2mol电子时,反应的Cu为0.1mol,其质量为6.4g,
故答案为:Cu;6.4;
(3)铝片和铜片插入浓HNO3溶液中,金属铝会钝化,金属铜和浓硝酸之间会发生自发的氧化还原反应,此时金属铜时负极,金属铝是正极;
插入稀NaOH溶液中,金属铜和它不反应,金属铝能和氢氧化钠发生自发的氧化还原反应,此时金属铝是负极,金属铜是正极,
故答案为:B;
(4)①氢氧燃料电池的总反应即是氢气与氧气反应生成水,其反应的总方程式为:2H2+O2=2H2O,
故答案为:2H2+O2=2H2O;
②已知氢氧燃料电池的总反应为:2H2+O2=2H2O,电池工作一段时间后,生成水使溶液体积增大,则硫酸的浓度减小,
故答案为:减小.
点评 本题考查了原电池原理的应用,涉及电极判断与电极反应式书写等问题,做题时注意从氧化还原的角度判断原电池的正负极以及电极方程式的书写,本题中难点和易错点为电极方程式的书写.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
17.下列分子中,属于含有非极性键的分子是( )
| A. | H2O | B. | Cl2; | C. | CCl4; | D. | CO2 |
15.铅酸蓄电池是目前应用普遍的化学电池,新型液流式铅酸蓄电池以可溶的甲基磺酸铅为电说解质,电池总反应:Pb+PbO2+4H+$?_{充电}^{放电}$ 2Pb2++2H2O,下列有关新型液流式铅酸蓄电池的法不正确的是( )
| A. | 放电时,蓄电池由化学能转化为电能 | |
| B. | 充放电时,溶液的导电能力变化不大 | |
| C. | 放电时的负极反应式为 Pb-2e-═Pb2+ | |
| D. | 充电时的阳极反应式为 Pb2++4OH-+2e-═PbO2+2H2O |
2.已知:①硫酸比次氯酸稳定;②高氯酸是比硫酸更强的酸;③S2-比Cl-易被氧化;④HCl比H2S稳定;⑤铜与盐酸不反应,与浓H2SO4能反应.可说明氯比硫的非金属性强的是( )
| A. | 全部 | B. | ②③④ | C. | ①②④ | D. | ②③④⑤ |
19.除去下列括号内的杂质,所选用的试剂和分离方法能达到实验目的是( )
| 选项 | 混合物 | 试剂(足量) | 分离方法 |
| A | 苯(苯酚) | 浓溴水 | 过滤 |
| B | 乙烷(乙烯) | 酸性KMnO4溶液 | 洗气 |
| C | 乙酸乙酯(乙酸) | 饱和Na2CO3溶液 | 分液 |
| D | 乙酸(乙醛) | 新制Cu(OH)2悬浊液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
16.甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时放出222.5kJ热量,则下列热化学方程式中正确的是( )
| A. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-22.5kJ•mol-1 | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=+890kJ•mol-1 | |
| C. | 2CH4(g)+4O2(g)═2CO2(g)+4H2O(l)△H=-890kJ•mol-1 | |
| D. | 2CH4(g)+4O2(g)═2CO2(g)+4H2O(l)△H=-1780kJ•mol-1 |
17.分子式为C8H11N的所有芳香族化合物的同分异构体共有( )种.
| A. | 15 | B. | 16 | C. | 19 | D. | 20 |