题目内容
16.下列物质中能与NaOH溶液、Na2CO3、溴水、苯酚钠溶液和甲醇都反应的是( )| A. | C6H6 | B. | CH3CHO | C. | CH3COOH | D. | CH2=CH-COOH |
分析 与NaOH溶液、Na2CO3反应,具有酸性,含酚-OH或-COOH,与苯酚钠水溶液反应,则酸性大于苯酚,与溴水反应可能含双键,与甲醇反应含-COOH,以此解答.
解答 解:A.C6H6与NaOH溶液、Na2CO3、溴水、苯酚钠水溶液和甲醇均不反应,故A不选;
B.CH3CHO与NaOH溶液、Na2CO3、苯酚钠水溶液和甲醇均不反应,故B不选;
C.CH3COOH与溴水不反应,故C不选;
D.CH2=CH-COOH中含-COOH,与NaOH溶液、Na2CO3、苯酚钠水溶液和甲醇反应,含双键与溴水发生加成反应,故D选;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、羧酸性质的考查,题目难度不大.

练习册系列答案
相关题目
6.短周期主族元素A、B、C、D,原子序数依次增大.A.C的原子序数的差为8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半.下列叙述正确的是( )
| A. | 原子半径:A<B<C<D | |
| B. | 非金属性:A>C | |
| C. | B和D最高价氧化物对应水化物相互不反应 | |
| D. | 单质B常温下能溶于浓硝酸 |
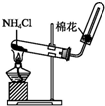
4.下列有关氨和铵盐的说法正确的是( )

| A. | 氨和铵盐都易溶于水,都能生成NH4+ | |
| B. | 铵态氮肥与碱性物质如草木灰混合施用肥效更高 | |
| C. | 实验室制备氨气的试剂和装置可为如图装置 | |
| D. | 工业上用氨气液化需吸收热量的过程做制冷剂 |
11.检验牙膏中是否含有甘油选用的试剂是( )
| A. | 氢氧化钠溶液 | B. | 新制氢氧化铜浊液 | ||
| C. | 醋酸溶液 | D. | 碳酸钠溶液 |
11.已知 25℃时部分弱电解质的电离平衡常数数据如表:
回答下列问题:
(4)写出碳酸的第一级电离平衡常数表达式:K1=$\frac{[HC{{O}_{3}}^{-}]•[{H}^{+}]}{[{H}_{2}C{O}_{3}]}$.
(2)25℃时,等物质的量浓度的 a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的 pH 由大到小的顺序为cbda (填字母).
(3)常温下,0.1mol•L-1的 CH3COOH 溶液加水稀释过程中,下列表达式的数据变大的是BD(填序号)
A.[H+]B.$\frac{{H}^{+}}{C{H}_{3}COOH}$ C.[H+]•[OH-]D.$\frac{O{H}^{-}}{{H}^{+}}$
(4)25℃时,将 20mL 0.1 mol•L-1 CH3COOH 溶液和 20mL 0.1 mol•L-1HSCN 溶液分别与 20mL 0.1 mol•L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图1所示:反应初始阶段两种溶液产生 CO2气体的速率存在明显差异的原因是HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快,反应结束后所得两溶液中,c(CH3COO-)<c(SCN-)(填“>”、“<”或“=”).

(5)体积均为 100mL pH=2 的 CH3COOH 与一元酸 HX,加水稀释过程中 pH 与溶液体积的关系如图2所示,则 HX 的电离平衡常数小于(填“大于”、“小于”或“等于”)CH3COOH 的电离平衡常数.
(6)25℃时,在 CH3COOH 与 CH3COONa 的混合溶液中,若测得 pH=6,
则溶液中 c(CH3COO-)-c(Na+)=9.9×10-7 mol•L-1(填精确值),$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=18.
(7)写出少量 CO2通入次氯酸钠溶液中的离子方程式:CO2+H2O+ClO-=HCO3-+HClO.
| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10 -1 | 1.7×10 -5 | 6.2×10 -10 | K1=4.3×10-7 K2=5.6×10-11 |
(4)写出碳酸的第一级电离平衡常数表达式:K1=$\frac{[HC{{O}_{3}}^{-}]•[{H}^{+}]}{[{H}_{2}C{O}_{3}]}$.
(2)25℃时,等物质的量浓度的 a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的 pH 由大到小的顺序为cbda (填字母).
(3)常温下,0.1mol•L-1的 CH3COOH 溶液加水稀释过程中,下列表达式的数据变大的是BD(填序号)
A.[H+]B.$\frac{{H}^{+}}{C{H}_{3}COOH}$ C.[H+]•[OH-]D.$\frac{O{H}^{-}}{{H}^{+}}$
(4)25℃时,将 20mL 0.1 mol•L-1 CH3COOH 溶液和 20mL 0.1 mol•L-1HSCN 溶液分别与 20mL 0.1 mol•L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图1所示:反应初始阶段两种溶液产生 CO2气体的速率存在明显差异的原因是HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快,反应结束后所得两溶液中,c(CH3COO-)<c(SCN-)(填“>”、“<”或“=”).

(5)体积均为 100mL pH=2 的 CH3COOH 与一元酸 HX,加水稀释过程中 pH 与溶液体积的关系如图2所示,则 HX 的电离平衡常数小于(填“大于”、“小于”或“等于”)CH3COOH 的电离平衡常数.
(6)25℃时,在 CH3COOH 与 CH3COONa 的混合溶液中,若测得 pH=6,
则溶液中 c(CH3COO-)-c(Na+)=9.9×10-7 mol•L-1(填精确值),$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=18.
(7)写出少量 CO2通入次氯酸钠溶液中的离子方程式:CO2+H2O+ClO-=HCO3-+HClO.
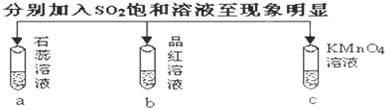
 ,它可通过不同化学反应分别制得B、C、D和E四种物质.
,它可通过不同化学反应分别制得B、C、D和E四种物质.
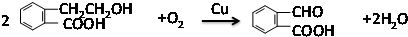 ;氧化反应;
;氧化反应; ;酯化反应;
;酯化反应; $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ .
.