题目内容
7.下列实验报告记录的实验现象正确的是( )| 实验 | 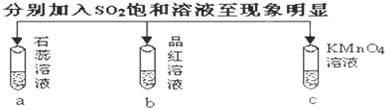 | |||
| 记录 | A | 无色 | 无色 | 无色 |
| B | 红色 | 无色 | 无色 | |
| C | 无色 | 无色 | 紫色 | |
| D | 红色 | 无色 | 紫色 | |
| A. | A | B. | B | C. | C | D. | D |
分析 二氧化硫为酸性氧化物能够与水反应生成亚硫酸,溶液显酸性,具有漂白性能够使品红褪色,具有还原性,能够还原酸性的高锰酸钾,以此解答该题.
解答 解:二氧化硫为酸性氧化物能够与水反应生成亚硫酸,溶液显酸性,能够使石蕊试液变红色;具有漂白性能够使品红褪色;具有还原性,能够还原酸性的高锰酸钾,使高锰酸钾褪色;
所以abc中颜色变化为:红色、无色、无色;
故选B.
点评 本题考查二氧化硫的性质,为高频考点,侧重于双基的考查,熟悉发生的化学反应是解答本题的关键,注意二氧化硫与氯水溶液反应是学生解答的难点,题目难度不大.

练习册系列答案
 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
18.辉铜矿是一种重要的铜矿石,主要含有硫化亚铜(Cu2S),还有Fe2O3、SiO2及一些不溶性杂质.一种以辉铜矿石为原料制备硝酸铜晶体的工艺流程如下:
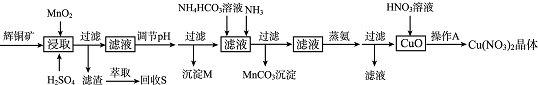
已知:部分金属阳离子生成氢氧化物沉淀的pH范围如下表所示(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
回答下列问题:
(1)浸取后得到的浸出液中含有CuSO4、MnSO4.写出浸取时产生CuSO4、MnSO4反应的化学方程式2MnO2+Cu2S+4H2SO4=S↓+2CuSO4+2MnSO4+4H2O.
(2)调节pH的目的是铁离子转化成氢氧化铁完全沉淀,pH的调节范围为3.2≤pH<4.4.
(3)生成MnCO3沉淀的离子方程式为Mn2++NH3+HCO3-=MnCO3↓+NH4+.
(4)操作A为蒸发浓缩、冷却结晶.
(5)由辉铜矿制取铜的反应过程可以表示为:
2Cu2S(s)+3O2 (g)=2Cu2O(s)+2SO2(g)△H=-768.2kJ•mol-l
2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g)△H=+116.0 kJ•mol-l
则由Cu2S与O2加热反应生成Cu的热化学方程式为Cu2S(s)+02(g)═2Cu(s)+SO2(g)△H=-217.4kJ.mol-l .
(6)若用含85% Cu2S的辉铜矿来制备无水Cu(NO3)2.假设浸取率为95%,调节pH时损失Cu 3%,蒸氨过程中有5%未转化为CuO,其它过程中无损耗,则1.0kg这样的辉铜矿最多能制备1.75kg无水Cu(NO3)2.

已知:部分金属阳离子生成氢氧化物沉淀的pH范围如下表所示(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
| 离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
(1)浸取后得到的浸出液中含有CuSO4、MnSO4.写出浸取时产生CuSO4、MnSO4反应的化学方程式2MnO2+Cu2S+4H2SO4=S↓+2CuSO4+2MnSO4+4H2O.
(2)调节pH的目的是铁离子转化成氢氧化铁完全沉淀,pH的调节范围为3.2≤pH<4.4.
(3)生成MnCO3沉淀的离子方程式为Mn2++NH3+HCO3-=MnCO3↓+NH4+.
(4)操作A为蒸发浓缩、冷却结晶.
(5)由辉铜矿制取铜的反应过程可以表示为:
2Cu2S(s)+3O2 (g)=2Cu2O(s)+2SO2(g)△H=-768.2kJ•mol-l
2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g)△H=+116.0 kJ•mol-l
则由Cu2S与O2加热反应生成Cu的热化学方程式为Cu2S(s)+02(g)═2Cu(s)+SO2(g)△H=-217.4kJ.mol-l .
(6)若用含85% Cu2S的辉铜矿来制备无水Cu(NO3)2.假设浸取率为95%,调节pH时损失Cu 3%,蒸氨过程中有5%未转化为CuO,其它过程中无损耗,则1.0kg这样的辉铜矿最多能制备1.75kg无水Cu(NO3)2.
2.下列物质属于分子晶体的化合物的是( )
| A. | 石英 | B. | 氯化钠 | C. | 干冰 | D. | 钠 |
12.下列各组离子中能在水溶液中大量共存,且溶液呈酸性的是( )
| A. | Na+、K+、HCO3-、NO3- | B. | H+、Na+、Cl-、 | ||
| C. | Fe3+、K+、S2-、Cl- | D. | Cu2+、NO3-、Mg2+、SO42- |
19.由CO2、H2和CO组成的混合气体在同温、同压下与氮气的密度相同,则该混合气体中CO2、H2和CO的体积比为( )
| A. | 19:8:13 | B. | 22:1:14 | C. | 13:9:29 | D. | 26:16:27 |
16.下列物质中能与NaOH溶液、Na2CO3、溴水、苯酚钠溶液和甲醇都反应的是( )
| A. | C6H6 | B. | CH3CHO | C. | CH3COOH | D. | CH2=CH-COOH |
2.H、C、N、O、Na、S、Cl是常见的七种短周期元素.
(1)N位于元素周期表第二 周期第ⅤA 族,其基态原子核外有3个未成对电子;S的基态原子核外电子排布式为1s22s22p63s23p4.
(2)用“>”或“<’’填空:
(3)由上述元素中的任意两种元素组成的化合物中,既含极性键又含非极性键的物质有H2O2、N2H4、C2H2、C2H4、C2H6、C6H6等任选其一(任写一种物质的分子式).
(4)NH3可作低温溶剂,它易液化的原因是NH3分子间能形成分子间氢键,氢键的存在使得氨气分子间作用力显著增强,沸点显著升高,易液化.已知25℃、101KPa,NH3能在纯氧中燃烧,每转移1mol e-,放出akJ热量,写出该条件下NH3燃烧的热化学方程式4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-4a kJ/mol.
(5)通常情况下,N2O5为无色晶体,它与Na2O2能发生反应(类似于CO2与Na2O2能反应),写出反应的化学方程式,并用单线桥标出电子转移的方向和数目: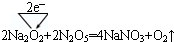 .
.
(1)N位于元素周期表第二 周期第ⅤA 族,其基态原子核外有3个未成对电子;S的基态原子核外电子排布式为1s22s22p63s23p4.
(2)用“>”或“<’’填空:
| 第一电离能 | 电负性 | 稳定性 | 酸性 |
| N>O | C<N | H2S<H2O | H2SO4<HClO4 |
(4)NH3可作低温溶剂,它易液化的原因是NH3分子间能形成分子间氢键,氢键的存在使得氨气分子间作用力显著增强,沸点显著升高,易液化.已知25℃、101KPa,NH3能在纯氧中燃烧,每转移1mol e-,放出akJ热量,写出该条件下NH3燃烧的热化学方程式4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-4a kJ/mol.
(5)通常情况下,N2O5为无色晶体,它与Na2O2能发生反应(类似于CO2与Na2O2能反应),写出反应的化学方程式,并用单线桥标出电子转移的方向和数目:
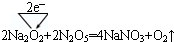 .
.