题目内容
电子表用的微型电池是利用氧化还原反应Ag2O+Zn=ZnO+2Ag来设计的,此反应的氧化剂为 ,被氧化的元素是 ,如果0.65g Zn参加反应,则转移的电子为 mol.
考点:原电池和电解池的工作原理
专题:电化学专题
分析:该原电池中,Zn元素化合价由0价变为+2价、Ag元素化合价由+1价变为0价,失电子化合价升高的反应物是还原剂、得电子化合价降低的反应物是氧化剂,氧化剂被还原、还原剂被氧化,根据锌和转移电子之间的关系式计算.
解答:
解:该原电池中,Zn元素化合价由0价变为+2价、Ag元素化合价由+1价变为0价,失电子化合价升高的反应物是还原剂、得电子化合价降低的反应物是氧化剂,氧化剂被还原、还原剂被氧化,所以氧化剂是Ag2O,被氧化的元素是Zn,参加反应的锌的物质的量=
=0.01mol,根据锌和转移电子之间的关系式得转移电子的物质的量=2n(Zn)=0.01mol×2=0.02mol,
故答案为:Ag2O;Zn;0.02.
| 0.65g |
| 65g/mol |
故答案为:Ag2O;Zn;0.02.
点评:本题以原电池为载体考查氧化还原反应,侧重考查基本概念及计算,明确氧化剂、还原剂的判断方法及各个物理量之间的关系即可解答,题目难度不大.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)?2NH3(g)△H=-92.6kJ/moL.实验测得起始、平衡时有关数据如下表:下列叙述错误的是( )
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
| A、容器①、②中反应达平衡时,状态完全相同 |
| B、①平衡时,N2的转化率为25% |
| C、容器②中达平衡时放出的热量Q<23.15 kJ |
| D、若向容器①加入2molN2、6molH2,则平衡时放出的热量23.15kJ<Q1<46.3 kJ |
下列各项表达中正确的是( )
A、-CH3(甲基)的电子式: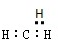 |
B、硝基苯的结构简式: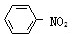 |
C、甲醛的结构式: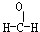 |
D、聚丙烯的结构简式: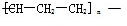 |
下列拟采用的金属防腐措施,不正确的是( )
| A、给金属衣架或电线外面包上一层塑料层 |
| B、给自行车钢圈镀上一层金属铬 |
| C、在铁船身上镶嵌金属铜 |
| D、给铁栅栏表面涂上一层油漆 |
下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A、1 mol聚乙烯含有的原子数目为6NA |
| B、标况下1L己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA/22.4 |
| C、1 mol甲基含9NA个电子 |
| D、2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |