题目内容
将一小块钠投入滴有石蕊的水中,下列有关现象的叙述错误的是( )
| A、钠浮在液面上 |
| B、有无色无味的气体产生 |
| C、水溶液变为蓝色 |
| D、水溶液变为红色 |
考点:钠的化学性质
专题:金属概论与碱元素
分析:钠的密度小于水,钠的熔点较低,钠和水剧烈反应生成氢氧化钠和氢气,且反应放出大量的热,氢氧化钠溶液呈碱性,紫色石蕊试液遇碱变蓝色.
解答:
解:A.钠的密度小于水,所以钠会浮在液面上,故A正确;
B.钠和水反应2Na+2H2O=2NaOH+H2↑,生成氢氧化钠和氢气,所以有无色无味的气体产生,故B正确;
C.钠和水反应生成氢氧化钠和氢气,氢氧化钠溶液呈碱性,紫色石蕊试液遇碱变蓝色,故C正确;
D.钠和水反应生成氢氧化钠和氢气,氢氧化钠溶液呈碱性,紫色石蕊试液遇碱变蓝色,不是红色,故D错误;
故选D.
B.钠和水反应2Na+2H2O=2NaOH+H2↑,生成氢氧化钠和氢气,所以有无色无味的气体产生,故B正确;
C.钠和水反应生成氢氧化钠和氢气,氢氧化钠溶液呈碱性,紫色石蕊试液遇碱变蓝色,故C正确;
D.钠和水反应生成氢氧化钠和氢气,氢氧化钠溶液呈碱性,紫色石蕊试液遇碱变蓝色,不是红色,故D错误;
故选D.
点评:本题考查了钠和水的反应,根据钠的物理性质、化学性质来分析解答,题目难度不大.

练习册系列答案
相关题目
水热法制备纳米颗粒Y(化合物)的反应为:3Fe2++2S2O32-+O2+4OH-═Y+S4O62-+2H2O,下列有关说法正确的是( )
| A、Y的化学式为Fe2O3 |
| B、S4O62-是还原产物 |
| C、被1mol O2氧化的Fe2+物质的量为1mol |
| D、每 32 gO2参加反应,转移电子的物质的量为4mol |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、NA个氧分子与NA个氢分子的质量比是16:1 |
| B、18克水所含电子数为NA |
| C、19.6g硫酸所含的硫原子数为0.1 NA |
| D、2.4g镁变成镁离子时,失去电子数目为0.1 NA |
如表是元素周期表的一部分,X、Y、Z、W均为短周期元素,X、Z的质子数之和为21.下列说法正确的是( )
| X | Y | ||
| Z | W |
| A、W元素的氢化物分子间有氢键 |
| B、Z和X能以共价键结合形成一种无机非金属材料 |
| C、Y元素的最高价氧化物的水化物是含氧酸中酸性最强的 |
| D、X元素的非金属性比Y元素非金属性强 |
下列关于蛋白质的叙述中,不正确的是( )
| A、蛋白质水解的最终产物为葡萄糖 |
| B、酒精消毒的原理是酒精能使蛋白质变性 |
| C、重金属盐能使蛋白质变性凝结,所以误食重金属盐会中毒 |
| D、浓硝酸溅在皮肤上,使皮肤呈黄色是由于浓硝酸和蛋白质发生了颜色反应 |
钠在自然界中最主要的存在形式是( )
| A、游离态 | B、氯化钠 |
| C、硫酸钠 | D、硝酸钠 |
下列变化过程中△H<0的是( )
| A、电解Al2O3得到Al和O2 |
| B、HCl分解为H2和Cl2 |
| C、焦碳与水蒸气反应 |
| D、Na与水反应 |
化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)?CuS(s)+Mn2+(aq),下列说法错误的是( )
| A、相同条件下,MnS的Ksp比CuS的Ksp大 | ||
B、该反应的平衡常数K=
| ||
| C、该反应达到平衡时c(Mn2+)=c(Cu2+) | ||
| D、往平衡体系中加入少量CuSO4固体后,c(Mn2+)变大 |
对下列说法不正确的是( )
| A、光化学烟雾的主要成分为氮的氧化物和碳氢化合物 |
| B、工业上可以从石油裂解气中获得乙烯 |
C、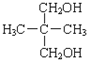 和 和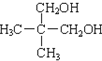 互为同分异构体 互为同分异构体 |
D、按系统命名法,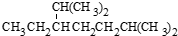 的名称为2,6-二甲基-3-乙基庚烷 的名称为2,6-二甲基-3-乙基庚烷 |