题目内容
12.在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)?zC(g),平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达到平衡时,测得A的浓度降低为0.30mol/L,则B的转化率变小,C的体积分数变小(填“变大”、“变小”或“不变”).分析 将容器的容积扩大到原来的两倍,若平衡不移动,A的浓度为0.25mol/L,而再达到平衡时,测得A的浓度降低为0.30mol/L,可知减小压强平衡逆向移动,以此解答该题.
解答 解:将容器的容积扩大到原来的两倍,若平衡不移动,A的浓度为0.25mol/L,而再达到平衡时,测得A的浓度降低为0.30mol/L,可知减小压强平衡逆向移动,则B的转化率变小,C的体积分数变小,故答案为:变小;变小.
点评 本题考查外界条件对平衡移动的影响,为高频考点,侧重考查学生的分析能力,题目难度不大,注意分析反应的特征为解答该题的关键.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
2.下列八种物质:①丙烯、②甲苯、③聚氯乙烯、④乙醇、⑤丙炔、⑥乙酸乙酯、⑦环己烯、⑧溴乙烷中既能使酸性高锰酸钾溶液褪色,又能使溴水因反应而褪色的是( )
| A. | ①③④⑤⑦ | B. | ②④⑤⑦ | C. | ④⑤ | D. | ①⑤⑦ |
3.下列反应最终没有固体析出的是( )
| A. | 向NaHCO3溶液中加入过量澄清石灰水 | |
| B. | 向饱和氢氧化钠溶液中加入钠单质 | |
| C. | 向氯化钡溶液中通入少量SO2 | |
| D. | 向饱和碳酸钠溶液中通入过量CO2 |
20.下列实验现象与氧化还原反应有关的是( )
| A. | 将NO2通入水中,气体由红棕色逐渐转变为无色 | |
| B. | 向澄清的石灰水中通入SO2,有白色沉淀形成 | |
| C. | NH3使湿润的红色石蕊试纸变蓝 | |
| D. | 向Fe2(SO4)3溶液中滴加NaOH溶液,生成红褐色沉淀 |
7.下列装置所示的实验中,能达到实验目的是( )
| A. | 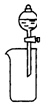 从Mg(OH)2悬浊液中分离出Mg(OH)2 | B. | 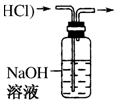 除去HCl中的SO2 | ||
| C. | 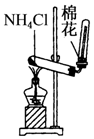 实验室制氨气 | D. | 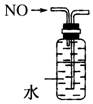 排水法收集NO |
17.化学与科学、技术、社会、环境密切相关,下列说法错误的是( )
| A. | 神舟九号升空时火箭发射的动力主要来源于化学能 | |
| B. | 洁厕灵的主要成分是盐酸,不能与“84”消毒液混用 | |
| C. | 采用催化转换技术将汽车尾气中的NOx和CO转化为无毒气体 | |
| D. | 高纯硅广泛应用于太阳能电池、计算机芯片和光导纤维 |
1.下列说法正确的是( )
| A. | 含碳元素的化合物都是有机物 | |
| B. | 苯的同系物能使KMnO4酸性溶液褪色 | |
| C. | 石油分馏可获得乙烯、丙烯和丁二烯 | |
| D. | 酯类和醇类均能发生水解反应 |
2.下列事实不能用勒夏特列原理解释的是( )
| A. | 溴水中有下列平衡Br2+H2O?HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 | |
| B. | 合成氨反应,为提高氨的产率,理论上应采取降低温度的措施 | |
| C. | 反应CO(g)+NO2 (g)?CO2 (g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深 | |
| D. | 对于2HI(g)?H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 |
