题目内容
7.下列分子或离子在指定的分散系中能大量共存的一组是( )| A. | 饱和氯水中:Na+、K+、Cl-、CO32- | |
| B. | 淀粉溶液中:K+、NH4+、SO42-、I- | |
| C. | Na2SiO3溶液中:Cl-、I-、K+、CO2 | |
| D. | 葡萄糖溶液中:Na+、H+、SO42-、Cr2O72- |
分析 A.氯水中含氢离子;
B.淀粉溶液为中性;
C.发生强酸制取弱酸的反应;
D.葡萄糖具有还原性,能被氧化.
解答 解:A.饱和氯水有强酸性,CO32-与之反应而不能大量共存,故A错误;
B.各离子都能与淀粉溶液不反应,可大量共存,故B正确;
C.CO2可与Na2SiO3溶液反应生成H2SiO3溶液沉淀而不能大量共存,故C错误;
D.Cr2O72-可将葡萄糖氧化而不能共存,故D错误;
故选B.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
17.氮氧化铝(AlON)是一种透明高硬度防弹材料,可以由反应Al2O3+C+N2=2AlON+CO(高温)合成,下列有关说法正确的是( )
| A. | 氮氧化铝中氮的化合价是-3 | |
| B. | 反应中每生成5.7g AlON的同时生成1.12 L CO | |
| C. | 反应中氮气作氧化剂 | |
| D. | 反应中氧化产物和还原产物的物质的量之比是2:1 |
18.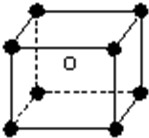 某离子化合物的晶胞如图所示立体结构,阳离子位于此晶胞的中心,阴离子位于8个顶点,该离子化合物中,阴、阳离子个数比是( )
某离子化合物的晶胞如图所示立体结构,阳离子位于此晶胞的中心,阴离子位于8个顶点,该离子化合物中,阴、阳离子个数比是( )
 某离子化合物的晶胞如图所示立体结构,阳离子位于此晶胞的中心,阴离子位于8个顶点,该离子化合物中,阴、阳离子个数比是( )
某离子化合物的晶胞如图所示立体结构,阳离子位于此晶胞的中心,阴离子位于8个顶点,该离子化合物中,阴、阳离子个数比是( )| A. | 1:8 | B. | 1:4 | C. | 1:1 | D. | 1:2 |
2.有5种短周期元素在周期表中位置如图所示.已知:X的氢化物可用于刻蚀普通玻璃.下列推断正确的是( )
| | | G | | X |
| R | T | Y |
| A. | R和Y组成的化合物水溶液呈中性 | |
| B. | 最高价氧化物的水化物酸性:Y>G>X>R | |
| C. | 简单氢化物稳定性:X>Y>T | |
| D. | 常温下,TX4、TY4都呈液态 |
12.下列各组数据中比值不为1:1的是( )
| A. | 100℃时,pH=6的纯水中,c(OH-)与c(H+)之比 | |
| B. | 常温下,pH=1的HF溶液与0.1mol•L-1的盐酸中c(H+)之比 | |
| C. | 常温下,pH=7的CH3COOH与CH3COONa的混合溶液中,c(CH3COO-)与c(Na+)之比 | |
| D. | 常温下,pH=12的Ba(OH)2溶液与pH=12的KOH溶液中溶质的物质的量浓度之比 |
19.室温下,将1molNa2CO3•10H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1molNa2CO3(s)溶于水会使溶液温度升高,热效应为△H2;Na2CO3•10H2O受热分解的化学方程为:Na2CO3•10H2O(s)$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3(s)+10H2O(l),热效应为△H3,则下列判断正确的是( )
| A. | △H2<△H3 | B. | △H1>△H3 | C. | △H1+△H3=△H2 | D. | △H1+△H2>△H3 |
16.下列关于化学键的叙述,正确的一项是( )
| A. | 离子化合物中一定含有离子键 | |
| B. | 单质分子中均存在化学键 | |
| C. | 含有非极性共价键的分子一定是单质分子 | |
| D. | 含有共价键的化合物一定是共价化合物 |
17.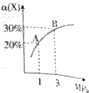 在一定条件下,反应X(g)+3Y(g)?2Z(g)△H=-92.4kJ•mol-1,X的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
在一定条件下,反应X(g)+3Y(g)?2Z(g)△H=-92.4kJ•mol-1,X的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
 在一定条件下,反应X(g)+3Y(g)?2Z(g)△H=-92.4kJ•mol-1,X的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
在一定条件下,反应X(g)+3Y(g)?2Z(g)△H=-92.4kJ•mol-1,X的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )| A. | 图中A、B两点,达到相同的平衡体系 | |
| B. | 上述反应在达到平衡后增大压强,X的转化率提高 | |
| C. | 升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小 | |
| D. | 将1.0molX,3.0molY,置于1L密闭容器中发生反应,放出的热量为92.4kJ |