题目内容
10.下列有关酸的事实和括号中对应表现出的性质均正确的是( )| A. | H2S气体能用浓硫酸进行干燥(浓硫酸的吸水性) | |
| B. | 铜与浓硝酸制备NO2气体(浓硝酸的强氧化性、酸性) | |
| C. | SO2的水溶液能够使品红溶液褪色(H2SO3的强氧化性) | |
| D. | 可口可乐瓶盖打开后,有大量气体逸出(H2CO3的挥发性) |
分析 A、H2S与浓硫酸发生氧化还原反应;
B、硝酸与铜反应氮的化合价部分变化;
C、SO2的水溶液能够使品红溶液褪色,体现二氧化硫的漂白性;
D、体现二氧化碳的溶解性.
解答 解:A、H2S与浓硫酸发生氧化还原反应,所以不能用浓硫酸干燥硫化氢,体现浓硫酸的强氧化性,故A错误;
B、硝酸与铜反应氮的化合价部分变化,所以体现浓硝酸的强氧化性和酸性,故B正确;
C、SO2的水溶液能够使品红溶液褪色,体现二氧化硫的漂白性,而不是H2SO3的强氧化性,故C错误;
D、可口可乐瓶盖打开后,有大量气体逸出,体现二氧化碳的溶解性减小,而不是H2CO3的挥发性,故D错误;
故选B.
点评 本题考查化学实验方案的评价,涉及氧化还原反应、二氧化硫和铝的溶解性等,熟悉物质的性质是解题关键,注意二氧化硫的还原性和漂白性,题目难度不大.

练习册系列答案
相关题目
7.化学实验是化学学科学习、探究的基础.
(1)下列描述错误的是acde.
a.为了防止试剂瓶内的试剂被污染,取用后多余的试剂一定都不能放回原试剂瓶
b.滴定管、容量瓶、分液漏斗在使用时都需要检漏
c.海带中碘的提取时需要对干海带进行灼烧,此时需要用到的仪器有玻璃棒、燃烧匙、泥三角、三脚架、酒精灯
d.检验Na2SO3固体是否被氧化:取少量固体溶于水,加入Ba(NO3)2溶液,产生白色沉淀,滴加稀盐酸,观察白色沉淀是否溶解
e.海带中碘的提取时,对碘水中的碘进行萃取可采用裂化汽油、苯、四氯化碳、无水酒精等有机溶剂
(2)某溶液中可能存在Br-、CO32-、SO32-、I-、A13+、Mg2+、Na+等7种离子中的某几种.现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,有白色沉淀生成,加入稀盐酸沉淀不溶解.
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.据此可以推断:该溶液肯定存在的离子是:CO32-、Br-、Na+、SO32-
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
①请完成此实验设计,其中:
V1=30,V6=10,V9=17.5;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因:当加入一定量的CuSO4后,生成的单质Cu会沉积在Zn的表面,降低了Zn与H2SO4溶液的接触面积而使反应速率下降.
(1)下列描述错误的是acde.
a.为了防止试剂瓶内的试剂被污染,取用后多余的试剂一定都不能放回原试剂瓶
b.滴定管、容量瓶、分液漏斗在使用时都需要检漏
c.海带中碘的提取时需要对干海带进行灼烧,此时需要用到的仪器有玻璃棒、燃烧匙、泥三角、三脚架、酒精灯
d.检验Na2SO3固体是否被氧化:取少量固体溶于水,加入Ba(NO3)2溶液,产生白色沉淀,滴加稀盐酸,观察白色沉淀是否溶解
e.海带中碘的提取时,对碘水中的碘进行萃取可采用裂化汽油、苯、四氯化碳、无水酒精等有机溶剂
(2)某溶液中可能存在Br-、CO32-、SO32-、I-、A13+、Mg2+、Na+等7种离子中的某几种.现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,有白色沉淀生成,加入稀盐酸沉淀不溶解.
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.据此可以推断:该溶液肯定存在的离子是:CO32-、Br-、Na+、SO32-
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
V1=30,V6=10,V9=17.5;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因:当加入一定量的CuSO4后,生成的单质Cu会沉积在Zn的表面,降低了Zn与H2SO4溶液的接触面积而使反应速率下降.
5.下列状态的物质,既能导电又属于电解质的是( )
| A. | MgCl2晶体 | B. | NaCl溶液 | C. | 液态HCl | D. | 熔融的NaOH |
15.钒是一种熔点很高的金属,具有良好的可塑性和低温抗腐蚀性,有延展性、硬度大,无磁性.广泛应用于钢铁、航空航天、能源、化工等领域.中铝集团 (平果铝业公司)目前使用一种新型工艺,以便从铝业生成的固体废料--赤泥中提取金属钒,具体工艺流程图如下:
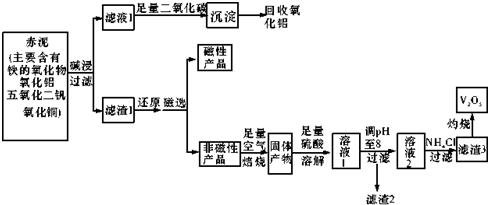
已知:I.钒有多种价态,其中+5价最稳定.钒在溶液中主要以V02+和V03-的形式存在,存在平衡V02++H20?V03-+2H+.
Ⅱ.部分含钒物质在水中的溶解性如下表所示:
Ⅲ.部分离子的沉淀pH值:
请回答下列问题:
(1)碱浸步骤中最好选用a.
a.Na0H溶液b.氨水 c.纯碱溶液
(2)写出滤液1与足量二氧化碳反应的离子方程式AlO2-+CO2+2H2O=Al(OH)3+HCO3-;.
(3)磁选步骤得到的磁性产品为铁.
(4)溶液1到溶液2的过程中,调节pH值至8有两个目的,一是除去铜离子,二是使使VO2+转化为VO3-.
(5)滤渣3的主要成分为NH4VO3,工业上常用铝热反应法由V205冶炼金属钒,请写出反应的化学方程式3V205+10Al$\frac{\underline{\;高温\;}}{\;}$6V+5Al203.

已知:I.钒有多种价态,其中+5价最稳定.钒在溶液中主要以V02+和V03-的形式存在,存在平衡V02++H20?V03-+2H+.
Ⅱ.部分含钒物质在水中的溶解性如下表所示:
| 物质 | V205 | NH4V03 | (V02)2S04 |
| 溶解性 | 难溶 | 难溶 | 易溶 |
| Cu2+ | Fe2+ | Fe3+ | |
| 开始沉淀pH值 | 5.2 | 7.6 | 2.7 |
| 完全沉淀pH值 | 6.4 | 9.6 | 3.7 |
(1)碱浸步骤中最好选用a.
a.Na0H溶液b.氨水 c.纯碱溶液
(2)写出滤液1与足量二氧化碳反应的离子方程式AlO2-+CO2+2H2O=Al(OH)3+HCO3-;.
(3)磁选步骤得到的磁性产品为铁.
(4)溶液1到溶液2的过程中,调节pH值至8有两个目的,一是除去铜离子,二是使使VO2+转化为VO3-.
(5)滤渣3的主要成分为NH4VO3,工业上常用铝热反应法由V205冶炼金属钒,请写出反应的化学方程式3V205+10Al$\frac{\underline{\;高温\;}}{\;}$6V+5Al203.
2.下列分子式表示的物质不具有同分异体的是( )
| A. | C3H7Cl | B. | C3H6 | C. | CF2Cl2 | D. | C4H6 |
 .
.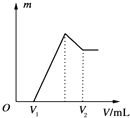 将0.1mol的镁、铝混合物溶于100mL、2mol•L-1的H2SO4溶液中,然后再滴加1mol•L-1的NaOH溶液.请回答:
将0.1mol的镁、铝混合物溶于100mL、2mol•L-1的H2SO4溶液中,然后再滴加1mol•L-1的NaOH溶液.请回答: