题目内容
某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、量筒、0.5mol?L-1 盐酸、0.55mol?L-1NaOH溶液,尚缺少的实验玻璃用品是 、 .
(2)实验中不能用环形铜丝搅拌棒代替环形玻璃搅拌棒,其原因是 .
(3)他们分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应.记录的实验数据如下:已知:Q=Cm(t2-t1),反应后溶液的比热容C为4.18kJ/(℃.kg),假设盐酸、NaOH溶液和反应后溶液的密度均为1g/cm3.
依据上述的实验数据计算,该实验测得的中和热△H= (结果保留一位小数)
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、量筒、0.5mol?L-1 盐酸、0.55mol?L-1NaOH溶液,尚缺少的实验玻璃用品是
(2)实验中不能用环形铜丝搅拌棒代替环形玻璃搅拌棒,其原因是
(3)他们分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应.记录的实验数据如下:已知:Q=Cm(t2-t1),反应后溶液的比热容C为4.18kJ/(℃.kg),假设盐酸、NaOH溶液和反应后溶液的密度均为1g/cm3.
| 实验序号 | 起始温度t1℃ | 终止温度t2℃ | |
| 盐酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
考点:中和热的测定
专题:实验设计题
分析:(1)根据中和热测定的实验步骤选用需要的仪器,然后判断还缺少的仪器;
(2)金属导热快,热量损失多;
(3)先根据表中测定数据计算出混合液反应前后的平均温度差,再根据Q=cm△T计算出反应放出的热量,最后计算出中和热;
(2)金属导热快,热量损失多;
(3)先根据表中测定数据计算出混合液反应前后的平均温度差,再根据Q=cm△T计算出反应放出的热量,最后计算出中和热;
解答:
解:(1)中和热的测定过程中,需要用量筒量取酸溶液、碱溶液的体积,需要使用温度计测量温度,所以还缺少温度计和量筒,
故答案为:量筒;温度计;
(2)不能用环形铜丝搅拌棒代替环形玻璃搅拌棒,因为铜丝搅拌棒是热的良导体,热量损失大,
故答案为:金属易导热,热量散失导致误差大;
(4)第1次实验盐酸和NaOH溶液起始平均温度为20.05℃,反应后温度为:23.2℃,反应前后温度差为:3.15℃;
第2次实验盐酸和NaOH溶液起始平均温度为20.3℃,反应前后温度差为:3.1℃;
第3次实验盐酸和NaOH溶液起始平均温度为20.55℃,反应前后温度差为:3.05℃;
40mL的0.50mol/L盐酸与40mL的0.55mol/L氢氧化钠溶液的质量和为m=80mL×1g/cm3=80g,c=4.18J/(g?℃),代入公式Q=cm△T得生成0.05mol的水放出热量
Q=4.18J/(g?℃)×80g×
=1.036kJ,即生成0.02mol的水放出热量为:1.036kJ,所以生成1mol的水放出热量为:1.036kJ×
=-51.8kJ/mol,即该实验测得的中和热△H=-51.8kJ/mol,
故答案为:-51.8kJ/mol;
故答案为:量筒;温度计;
(2)不能用环形铜丝搅拌棒代替环形玻璃搅拌棒,因为铜丝搅拌棒是热的良导体,热量损失大,
故答案为:金属易导热,热量散失导致误差大;
(4)第1次实验盐酸和NaOH溶液起始平均温度为20.05℃,反应后温度为:23.2℃,反应前后温度差为:3.15℃;
第2次实验盐酸和NaOH溶液起始平均温度为20.3℃,反应前后温度差为:3.1℃;
第3次实验盐酸和NaOH溶液起始平均温度为20.55℃,反应前后温度差为:3.05℃;
40mL的0.50mol/L盐酸与40mL的0.55mol/L氢氧化钠溶液的质量和为m=80mL×1g/cm3=80g,c=4.18J/(g?℃),代入公式Q=cm△T得生成0.05mol的水放出热量
Q=4.18J/(g?℃)×80g×
| 3.15℃+3.1℃+3.05℃ |
| 3 |
| 1mol |
| 0.02mol |
故答案为:-51.8kJ/mol;
点评:本题考查中和热的测定以及反应热的计算,题目难度中等,理解中和热测定原理是解答关键,试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
相关题目
人体血液的PH为维持在7.35~7.45,适量的CO2对维持这个PH变化范围其主要作用,其原理可用化学方程式表示:H2O+CO2=H++HCO3-.又知人体在正常情况下呼出的气体中CO2的体积分数约为5%,下了说法中正确的是( )
| A、安静状态下,长时间太快且太深的呼吸可以使呼出的气体中CO2的体积分数大于5% |
| B、人在痛苦中,长时间太深的呼吸可导致血液PH降低 |
| C、人在安静状态下,长时间太浅的呼吸可以导致血液PH降低 |
| D、窒息而死的人血液PH高于7.45 |
 某物质的晶体中含Ti、O、Ca三种元素,其晶胞排列方式如图所示,晶体中Ti、O、Ca的中原子个数之比为( )
某物质的晶体中含Ti、O、Ca三种元素,其晶胞排列方式如图所示,晶体中Ti、O、Ca的中原子个数之比为( )| A、1:3:1 |
| B、2:3:1 |
| C、2:2:1 |
| D、1:3:3 |
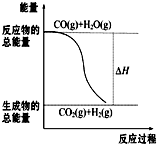 燃烧热是指一定条件下1mol可燃物完全燃烧生成稳定的氧化物时放出的热量.已知热化学方程式:①CO(g)+
燃烧热是指一定条件下1mol可燃物完全燃烧生成稳定的氧化物时放出的热量.已知热化学方程式:①CO(g)+| 1 |
| 2 |
| 1 |
| 2 |
| A、由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41.2 kJ?mol-1 | ||
| B、H2的燃烧热为241.8 kJ?mol-1 | ||
| C、H2(g)转变成H2O(g)的化学反应一定要释放能量 | ||
D、根据②推知反应H2(g)+
|