题目内容
【化学与技术】
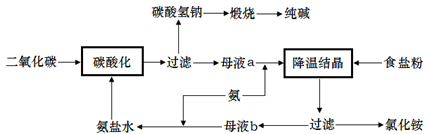
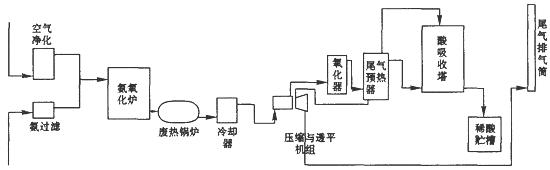
工业上制取硝酸铵的流程图如下,请回答下列问题:
(1)在上述工业制硝酸的生产中,B设备的名称是 ,其中发生反应的化学方程式为 。
(2)此生产过程中,N2与H2合成NH3所用的催化剂是 。1909年化学家哈伯在实验室首次合成了氨,2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如下:
 分别表示N2、H2、NH3。图⑤表示生成的NH3离开催化剂表面,图②和③的含义分别是 、 。
分别表示N2、H2、NH3。图⑤表示生成的NH3离开催化剂表面,图②和③的含义分别是 、 。
(3)在合成氨的设备(合成塔)中,设置热交换器的目的是 ;在合成硝酸的吸收塔中通入空气的目的是 。
(4)生产硝酸的过程中常会产生一些氮的氧化物,可用如下两种方法处理:
碱液吸收法:NO+NO2+2NaOH=2NaNO2+H2O
NH3还原法:8NH3+6NO2催化剂△ 7N2+12H2O(NO也有类似的反应)
以上两种方法中,符合绿色化学的是 。
(5)某化肥厂用NH3制备NH4NO3。已知:由NH3制NO的产率是96%、NO制HNO3的产率是92%,则制HNO3所用去的NH3的质量占总耗NH3质量(不考虑其它损耗)的 %。
(6)硝酸铵是一种常用的氮肥,在贮存和使用该化肥时,应注意的事项及理由是:
| | 注意事项 | 理由 |
| ① | | |
| ② | | |
(1)氧化炉,4NH3+5O2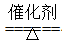 4NO+6H2O
4NO+6H2O
(2)铁砂网(或铁)。N2、H2被吸附在催化剂表面;在催化剂表面,N2、H2中化学键断裂
(3)利用余热,节约能源;使NO循环利用,全部转化成HNO3
(4)NH3还原法
(5)53
(6)①不能与碱性肥料混施;硝酸铵溶液呈酸性;
②不能剧烈撞击;硝酸铵易爆炸;
③不能在雨水较多的地区使用 硝酸铵吸收性强,易流失。
解析

【化学与技术】
世界环保联盟建议全面禁止使用氯气用于饮用水的消毒,而建议采用高效“绿色”消毒剂二氧化氯。二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时要避免光照、震动或加热。实验室以电解法制备ClO2的流程如下:请回答下列问题。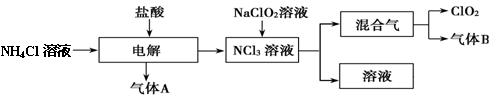
(1)ClO2中所有原子 (填“是”或“不是”)都满足8电子结构。上图所示电解法制得的产物中杂质气体B能使石蕊试液显蓝色,除去杂质气体可选用 。
A饱和食盐水 B碱石灰 C浓硫酸 D蒸馏水
(2)稳定性二氧化氯是为推广二氧化氯而开发的新型产品,下列说法正确的是 。
| A.二氧化氯可广泛用于工业和饮用水处理 |
| B.应用在食品工业中能有效地延长食品贮藏期 |
| C.稳定性二氧化氯的出现大大增加了二氧化氯的使用范围 |
| D.在工作区和成品储藏室内,要有通风装置和监测及警报装置 |
(4)我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式是 ,此法相比欧洲方法的优点是 。
(5)科学家最近又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学反应方程式为 ,此法提高了生产及储存、运输的安全性,原因是 。
科学家及一些实业家的贡献对科学的发展起着积极地推动作用。下列对有关科学家及其发明创造的叙述,错误的是
| A.拉瓦锡证明了化学反应中的质量守恒,建立了燃烧的新理论 |
| B.舍勒发现了氯气,凯库勒提出了苯的结构式 |
| C.侯德榜发明了“候氏制碱”法,吴蕴初开创了中国的氯碱工业 |
| D.道尔顿、汤姆孙、卢瑟福和门捷列夫等科学家对原子结构模型的建立均作出了卓越的贡献 |
下列说法不正确的是
| A.乙醇和二甲醚互为同分异构体,利用红外光谱法或核磁共振氢谱法均可鉴别两者 |
| B.乙酸乙醋在碱性条件下水解,属于皂化反应 |
| C.使用含有氯化钠的融雪剂会加快桥梁的腐蚀 |
| D.道尔顿首次提出原子学说、汤姆生发现电子、卢瑟福确定原子核的存在,都为原子结构理论的发展作出了巨大贡献 |

 2NH3(g) △H﹤0; 2SO2(g)+O2(g)
2NH3(g) △H﹤0; 2SO2(g)+O2(g)